
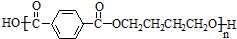
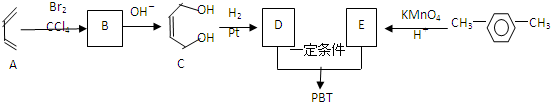
 互为同系物关系.
互为同系物关系.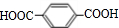 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$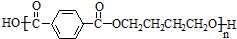 +(2n-1)H2O.
+(2n-1)H2O. 分析 1,3-丁二烯与溴发生加成反应生成B,B水解生成C,结合C的结构简式可知B为BrCH2CH=CHCH2Br,C与氢气发生加成反应生成D为HOCH2CH2CH2CH2OH,对二甲苯发生氧化反应生成E为 ,E与D发生缩聚反应得到
,E与D发生缩聚反应得到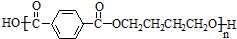 .
.
解答 解:1,3-丁二烯与溴发生加成反应生成B,B水解生成C,结合C的结构简式可知B为BrCH2CH=CHCH2Br,C与氢气发生加成反应生成D为HOCH2CH2CH2CH2OH,对二甲苯发生氧化反应生成E为 ,E与D发生缩聚反应得到
,E与D发生缩聚反应得到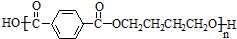 .
.
(1)A的系统命名为:1,3-丁二烯,它与 互为同系物,
互为同系物,
故答案为:1,3-丁二烯;同系物;
(2)A→B属于加成反应,B→C属于取代反应,
故答案为:加成反应;取代反应;
(3)B的结构简式(或键线式)为:BrCH2CH=CHCH2Br,同一不饱和碳原子上连接的原子或基团不同,它有顺反异构体.
故答案为:BrCH2CH=CHCH2Br;有;
(4)D+E→PBT的化学方程式:n HOCH2CH2CH2CH2OH+n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$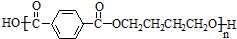 +(2n-1)H2O,
+(2n-1)H2O,
故答案为:n HOCH2CH2CH2CH2OH+n $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$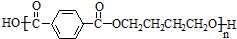 +(2n-1)H2O.
+(2n-1)H2O.
点评 本题卡插槽有机物的推断与合成,根据转化关系中有机物的结构与反应条件进行分析解答,需要学生熟练掌握官能团的性质与转化,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸钠 | B. | 硝酸银 | C. | 碳酸钠 | D. | 氯化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
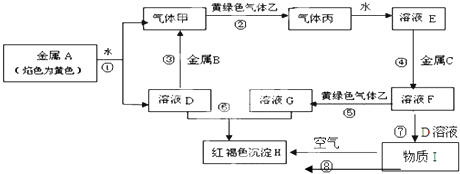
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
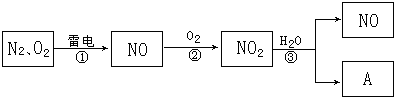
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
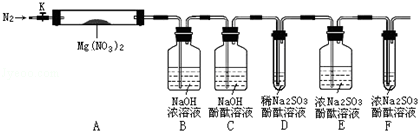
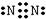 ,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.
,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
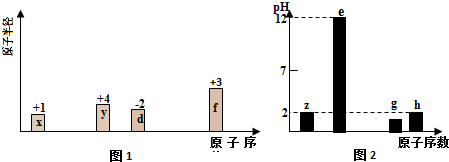
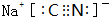 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com