
����Ŀ�����ȵ�ϡ�������ܽ���7.6gFeSO4���壬������50mL0.5mol��L-1KNO2��Һʱ�����е�Fe2+ȫ��ת����Fe3+��KNO2Ҳ��ȫ��Ӧ���ų�NxOy���塣
��1����ƽ�÷�Ӧ�ķ���ʽ__________________
FeSO4+ KNO2+ H2SO4![]() K2SO4+ Fe2(SO4)3+ ����+ H2O
K2SO4+ Fe2(SO4)3+ ����+ H2O
[��ѧ��������Ϊ��1����Ҳ����д����NxOyҪд���������ʲ���������]��
��2����Ӧ������������___________��
��3����״���£�������NxOy��������Ϊ2.24Lʱ��ת�Ƶĵ�����ĿΪ_____________��
���𰸡� 4 �� 2�� 3 ��1�� 2�� 1 N2O ��3 Fe2(SO4)3 0.4NA��2.408��1023
�����������⿼��������ԭ��Ӧ����ƽ�ͼ��㣬��1�����ݵ�ʧ������Ŀ�غ㣬��NO2����N����ԭ��x�ۣ���7.6��(3��2)/152=50��10��3��0.5��(3��x)�����x=1��NO2���Ļ�ԭ������N2O�����ݻ��ϼ۵�������������ƽ���÷�Ӧ����ʽΪ4FeSO4��2KNO3��3H2SO4=K2SO4��2Fe2(SO4)3��N2O����3H2O����2�����������ǻ�ԭ���������IJ������������ΪFe2(SO4)3����3������2.24LN2Oת�Ƶ������ʵ���Ϊ2.24��2��2/22.4mol=0.4mol����ת�Ƶ��Ӹ���Ϊ0.4NA��2.408��1023��


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.������ʱ�������Լ���ҩ����ҩ�ԣ�������ҽ������
B.ע����ù��ǰ��һ��Ҫ�Ƚ���Ƥ����������
C.���ڴ������ð�˾ƥ�ֿ�Ԥ��������û�и�����
D.��Ȼҩ�����β�������ҩ���ж�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С�������������о���
��1����ͬѧ����� A��B��C����ʵ����ͼ:

̽��������������������ϳ�ʱ���ͬѧ�۲쵽�������ǣ� A���������գ�b�����������⣻C�����������⡣
��ͨ������ʵ������������ɵó���������ⲿ������______________________________��
�����������绯ѧ��ʴ�������缫��ӦʽΪ______________________________��
��ʵ��B���õ�ˮҪ����________������ֲ���͵�������_________________��
��ʵ��C�м�ʯ�ҵ�������______________________��
��2����ͬѧΪ�˴ﵽͬ��Ŀ�ģ������ʵ��d��ͼ��ʾ��

����һ��ʱ����Թ��е�Һ�����{����ԭ����____________________________����ʵ��_______����ܡ����ܡ���˵��ˮ�������������Ӱ�졣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȼ��仯�����й㷺��;��
��1������������һ�����͵���������
��NaClO2��Cl�Ļ��ϼ�Ϊ____________��
��ʵ�������������Ũ���ᷴӦ�Ʊ�ClO2�������ClO2�⣬����Cl2��KCl�ȣ�д���÷�Ӧ�Ļ�ѧ����ʽ __________��������11.2L��������״������ת�Ƶ�����Ϊ _________��
��ClO2��Cl2������ʱ����������ԭΪCl�������³�ѹ�£��������ClO2������������Cl2��_________����
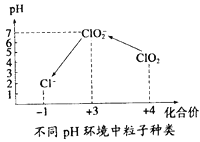
������ˮ����ClO2�������ˮ�У�Ҫ��ClO2��Ũ����0.1��0.8 mgL��1֮�䡣���������Լ��ˮ��ClO2��Ũ�ȣ���ͬpH����������������ͼ��ʾ�����������£�
��.ȡһ�������ˮ��������һ�����ĵ⻯�أ��ٽ���Ӧ����Һ�������ԣ������������Һ����Һ������
��.����һ������Na2S2O3��Һ������֪��2S2O32��+I2�TS4O62��+2I����
��.���������ˮ��pH��1��3��
���ʴ�
��ˮ�������Ϊ1.0L���ڲ���IIʱ������1.0��10��3molL��1��Na2S2O3��Һ10mL����ˮ����ClO2��Ũ����_____ mgL��1��
��2��ICl��ICl3�Ļ�ѧ������±�����ƣ�����Ϊ±�ػ�������Ȼ��⣨ICl3������ClΪ-1�ۣ����Զ������I2Cl6��ʽ���ڣ����絼�Dzⶨ֪�����ܷ������ֵ��룬���ɵ��������ӵ�Ħ�������ֱ�Ϊ198 g/mol��269 g/mol��������뷽��ʽΪ ________________ ��
��3����ʢ��һ�������廯������Һ�����Ȼ�̼��Һ���Թ��г���ͨ����������Ӧ��Ϻ������á��ֲ㣬�����л���ʺ���ɫ��������������BrCl������ClΪ-1�ۣ������ܷ������·�Ӧ��
��2Br��+Cl2=2Cl��+Br2 ��Br2+Cl2=2BrCl ��2Fe2��+Cl2=2Fe3��+2Cl��
��ͨ�������������Ⱥ�Ӧ��˳��Ϊ ____________������ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ��ˮ�ķ����Թ��У����Ϊ�����ֱ����ֱ�����͡������ƾ���NaBr��Һ�����ã�������ȷ����
A.������Һ�ֲ㣬�²���Ϻ�ɫ
B.������Һ�ֲ㣬�ϲ���Ϻ�ɫ
C.������Һ�ֲ㣬�²�ʻƺ�ɫ
D.������Һ���ֲ㣬��Һ�ɻƺ�ɫ��ɻ���ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪RxO![]() ��MnO
��MnO![]() ��H���D��RO2��Mn2����H2O�仯�����У�0.2 mol RxO
��H���D��RO2��Mn2����H2O�仯�����У�0.2 mol RxO![]() �μӷ�Ӧ����ת��0.4 mol ���ӡ�
�μӷ�Ӧ����ת��0.4 mol ���ӡ�
��1����Ӧ����������Ϊ________��
��2��x��________��
��3���μӷ�Ӧ�������ӵ����ʵ���Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С�������ղ���һ����������Ʒ��÷��������Ա���ʮ����á��÷���δ��ʴ����Ҫԭ���ǣ� ��
A.����������ѧ��ӦB.�����ױ�����
C.������������������ԭ��ӦD.���������������������б����ڲ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˷�ֹ����Ʒ��ʴ�����д�ʩ���������������� �� ��
A. ��ʹ�ú�IJ˵�ϴ������ B. ����Ʒ���������Ӧ������
C. ������ˮ�ܱ����һ��п D. �������Ŵ�������Ϳ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NH3����ԭ��������(SCR)������ĿǰӦ����㷺���������������ѳ���������Ӧԭ����ͼ��ʾ��

(1)SCR�����е�������Ϊ__________________��
(2)��NO2��NO�����ʵ���֮��Ϊ1��1ʱ��������������һ�������·�����Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ________________________________________������3 mol���ӷ���ת��ʱ������뷴Ӧ��NO�����ʵ���Ϊ____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com