
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊不消失. | NaAlO2溶液 |
| B | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. | Ca(OH)2溶液 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、① | B、④ | C、①④⑤ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则一定有CO32- |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定有SO42- |
| C、分别含有Mg2+、Cu2+和Na+的三种盐酸盐溶液,用NaOH溶液就能一次鉴别开 |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳粉和氧气反应 |
| B、细铁丝在氧气中燃烧 |
| C、二氧化碳通入氢氧化钠溶液中 |
| D、铜和硝酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 足量的石灰浆 |
| 操作① |
| 适量盐酸 |
| 操作② |
| HCl气流 |
| 操作③ |
| 电解 |
| 操作④ |
| A、操作①发生的反应为非氧化还原反应 |
| B、若在实验室进行操作①只需要漏斗和烧杯两种玻璃仪器 |
| C、操作②是蒸发浓缩、冷却结晶 |
| D、在整个制备过程中,未发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶上一般标有规格、温度和刻度线 |
| B、容量瓶在使用前要检查是否漏水 |
| C、可将固体或浓溶液直接在容量瓶中溶解或稀释 |
| D、容量瓶不能加热,也不宜长时间储存所配溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
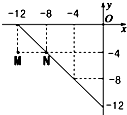 某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L.x与y的关系如图所示:
某温度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L.x与y的关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com