
 2SO3(g)����H<0��
2SO3(g)����H<0��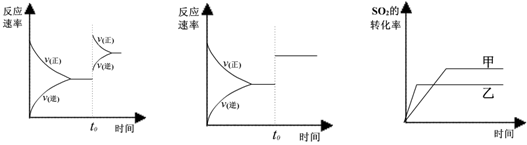
| A��ͼI�о�����t0ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� |
| B��ͼII�о�����t0ʱ�̼��������Է�Ӧ���ʵ�Ӱ�� |
| C��ͼIII�о����Ǵ�����ƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ� |
| D��ͼIII�о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϵ� |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ڢ� | B���ڢۢܢ� | C���٢ڢۢ� | D���ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)+2D(g) ��H<0����һ�������´ﵽƽ�⣬�����й�������ȷ����(�� ��)
C(g)+2D(g) ��H<0����һ�������´ﵽƽ�⣬�����й�������ȷ����(�� ��)| A���٢� | B���� | C���� | D���ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g)���ı�����������������߷�Ӧ���л���Ӱٷ������ǣ� ��
2SO3(g)���ı�����������������߷�Ӧ���л���Ӱٷ������ǣ� ��| A�������¶� | B������ѹǿ | C��ʹ�ô��� | D������Ӧ��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
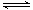 2SO3(g)����ƽ��ʱ����й��������±���
2SO3(g)����ƽ��ʱ����й��������±���| �� �� | �� | �� |
| ��Ӧ��Ͷ���� | 2 mol SO2��1 mol O2 | 4 mol SO3 |
| n(SO3)/mol | 1.6 | a |
| ��Ӧ���ת���� | ��1 | ��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1mol��L-1��min-1 | B��0.2mo1��L-1��min-1 |
| C��0.3mol��L-1��min-1 | D��0.4mo1��L-1��min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4NO��6H2O������Ӧ���ʷֱ���
4NO��6H2O������Ӧ���ʷֱ��� ��
�� ��
�� ��
�� [(mol / (L��min)]��ʾ������ȷ�Ĺ�ϵ�� ( )
[(mol / (L��min)]��ʾ������ȷ�Ĺ�ϵ�� ( ) A��4 ��5 ��5 | B��5 ��6 ��6 | C��2 ��3 ��3 | D��4 ��5 ��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
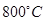 ʱ����ij��Ӧ�йص�����A��B��C�����ʵ���Ũ�ȴӿ�ʼ��Ӧ��4����ʱ�ı仯ͼ���Իش�
ʱ����ij��Ӧ�йص�����A��B��C�����ʵ���Ũ�ȴӿ�ʼ��Ӧ��4����ʱ�ı仯ͼ���Իش�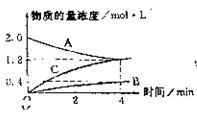
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com