
| A. | 寻找性能良好的新材料 | B. | 治理环境污染 | ||
| C. | 开发新能源 | D. | 研究质子、中子的结构 |
分析 根据化学的定义和研究内容进行分析判断,化学是一门在分子、原子的层次上研究物质的性质、组成、结构及其变化规律的科学,研究对象是物质,研究内容有组成、结构、性质、变化、用途等.
解答 解:A.寻找性能良好的新材料,属于研究、制取的物质,属于化学研究的范畴,故A错误;
B.治理环境污染,属于利用化学改善环境质量,属于化学研究的范畴,故B错误;
C.开发新能源,属于研究、制取的物质,属于化学研究的范畴,故C错误;
D.研究质子、中子的结构,属于物理研究的范畴,故D正确.
故选D.
点评 本题考查化学科学的主要研究对象,题目难度不大,了解化学研究的内容(物质的性质、组成、结构及其变化规律),才能利用化学知识服务于社会,造福于人类,有利于培养学生的学习兴趣,提高社会责任感.


科目:高中化学 来源: 题型:选择题
| A. | 生成气体体积为560mL | B. | 反应中电子转移数目为0.1NA | ||
| C. | Na2O2粉末中含离子数目为0.15NA | D. | 所得溶液pH为13 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
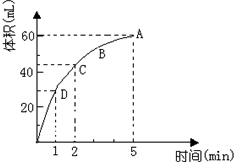 加入0.1mol的MnO2粉末于50mL过氧化氢的溶液中(密度为 1.1g/mL),在标准状况下放出气体的体积和时间的关系如图所示(假设溶液体积不变),回答下列问题:
加入0.1mol的MnO2粉末于50mL过氧化氢的溶液中(密度为 1.1g/mL),在标准状况下放出气体的体积和时间的关系如图所示(假设溶液体积不变),回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶用蒸馏水洗涤后,用待测HCl溶液润洗 | |
| B. | 滴定管用蒸馏水洗涤后,直接装入NaOH溶液进行滴定 | |
| C. | 滴定时,没有逐出滴定管下口的气泡 | |
| D. | 读数时,视线与滴定管内液体的凹液面最低处保持相平 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


| 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 不溶于水 |
| 对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 陈述I | 陈述II |
| A | 酸性:HCl>H2CO3 | 非金属性:Cl>C |
| B | K+、Ca2+、Mg2+ 的离子半径依次减小 | K+、Ca2+、Mg2+氧化性性依次增强 |
| C | 硬铝是合金 | 其熔点比金属铝的熔点低 |
| D | 电镀时阳极上发生还原反应 | 可在铁的镀件上镀铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(h) | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com