
| 1 |
| 10 |
| 1 |
| 10 |
| 0.01×126 |
| 6 |


科目:高中化学 来源: 题型:
| A、三种物质质子数之比为1:2:3 |
| B、三种物质中子数之比为1:1:1 |
| C、三种物质的摩尔质量之比为8:9:10 |
| D、三种物质的化学性质不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
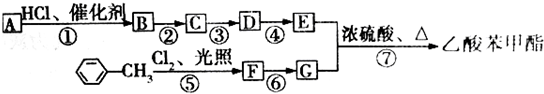
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CnH2n+2(n>1) |
| B、CnH2n(n>2) |
| C、CnH2n(n>1)和CmH2m(m>2) |
| D、CnH2n-2(n>1)与CmH2m-2(m,n>1) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 据报道“全国数以万计的高校、中学化学实验室每天都排放着成分复杂的污染物”.为此我校某化学兴趣小组拟进行如下实验,以粗略测试刚做完实验的实验室(甲)空气中全部酸性气体的含量.
据报道“全国数以万计的高校、中学化学实验室每天都排放着成分复杂的污染物”.为此我校某化学兴趣小组拟进行如下实验,以粗略测试刚做完实验的实验室(甲)空气中全部酸性气体的含量.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3OH |
| B、(CH3)3COH |
| C、CH3CHOHCH3 |
| D、CH3CH2CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、SO42-、Na+、Cl- |
| B、Na+、CO32-、H+、K+ Ba2+ |
| C、Ag+、NO3-、K+、Cl- |
| D、Mg2+、H+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com