
| ||
| ||


科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省如皋中学高二10月阶段练习化学试卷(带解析) 题型:填空题
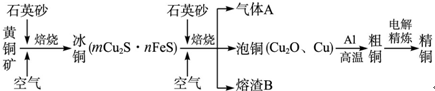
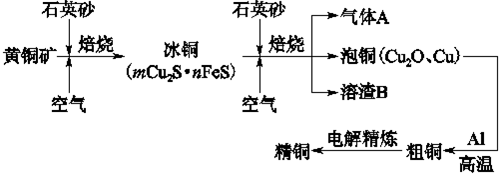
(12分)工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下: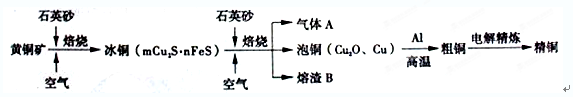
⑴气体A中的大气污染物可选用下列试剂中的____________吸收。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
⑵用稀H2SO4 浸泡熔渣B,取少量所得溶液,检验溶液中还存在Fe3+的方法是_______________________(注明试剂、现象)。
⑶由泡铜冶炼粗铜的化学反应方程式为__________________________________。
⑷以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是____________。
a.阴阳极的质量变化相等 b.电解质溶液的组成不发生变化
c.溶液中Cu2+向阳极移动 d.利用阳极泥可回收Ag、Pt、Au等金属
⑸利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com