
| A. | 118 | B. | 175 | C. | 47 | D. | 293 |
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解氯化铜溶液的阳极反应式为2Cl--2e-═Cl2↑ | |
| B. | 燃料电池负极加入或通入的物质是助燃物 | |
| C. | 原电池中电子从负极经过溶液流入正极 | |
| D. | 用惰性电极电解硝酸银溶液,一段时间后,溶液酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 由铜、锌和稀硫酸组成的原电池中:
由铜、锌和稀硫酸组成的原电池中:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-、Na+、H+ | B. | Cu2+、HCO3-、OH- | C. | OH-、A13+、SO42- | D. | Mg2+、Ca2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用NH4C1和Ca(OH)2反应制取NH3 | B. | 用浓盐酸和MnO2反应制取C12 | ||
| C. | 用H2O2溶液和MnO2反应制取O2 | D. | 用浓硝酸与Cu反应制取NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向MgCl2溶液中加入石灰乳:Mg2++2OH-═Mg(OH)2↓ | |
| B. | AlCl3溶液中滴加足量氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 将SO2通入氯水中:SO2+Cl2+2H2O═SO42-+2Cl-+4H+ | |
| D. | 向Ca(ClO)2溶液中通入过量CO2:2ClO-+CO2+H2O═2HClO+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
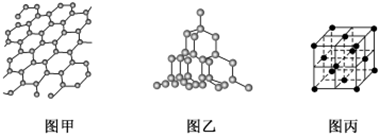
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com