
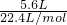 =0.25mol,故参加反应的HCl的物质的量为0.25mol×2=0.5mol,溶液中n(HCl)=0.3L×2mol/L=0.6mol,大于参加反应的HCl的物质的量,故金属完全反应,反应后溶液中加入一定量烧碱溶液,生成沉淀的质量最大,则镁离子、铝离子恰好完全转化为Mg(OH)2、Al(OH)3,则m(沉淀)=m(金属)+m(OH-),由生成的氢气的物质的量,根据电子注意守恒计算n(OH-),再根据m=nM计算m(OH-).
=0.25mol,故参加反应的HCl的物质的量为0.25mol×2=0.5mol,溶液中n(HCl)=0.3L×2mol/L=0.6mol,大于参加反应的HCl的物质的量,故金属完全反应,反应后溶液中加入一定量烧碱溶液,生成沉淀的质量最大,则镁离子、铝离子恰好完全转化为Mg(OH)2、Al(OH)3,则m(沉淀)=m(金属)+m(OH-),由生成的氢气的物质的量,根据电子注意守恒计算n(OH-),再根据m=nM计算m(OH-).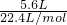 =0.25mol,故参加反应的HCl的物质的量为0.25mol×2=0.5mol,溶液中n(HCl)=0.3L×2mol/L=0.6mol,大于参加反应的HCl的物质的量,故金属完全反应,
=0.25mol,故参加反应的HCl的物质的量为0.25mol×2=0.5mol,溶液中n(HCl)=0.3L×2mol/L=0.6mol,大于参加反应的HCl的物质的量,故金属完全反应,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2009-2010学年湖南省长沙一中高三(上)第二次月考化学试卷(解析版) 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2011年江苏省南京市九校联合体高考调研化学试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com