
【题目】X、Y、Z三种元素的原子序数依次减小且三者原子序数之和为16,其常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法不正确的是( )
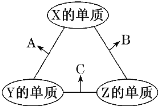
A.X元素位于VIA族B.1 molC中含有3mol共价键
C.A和C在一定条件下能发生氧化还原反应D.X与Y的最高正价大小:X>Y
【答案】D
【解析】
B和C均为10电子分子,考虑为氢化物,由转化关系可知,Z为氢,X、Y、Z原子序数之和为16,则X、Y的原子序数之和为15,原子序数X>Y,则Y为碳元素、X为氟元素或者Y为氮元素、X为氧元素,由转化关系,单质X、Y反应生成A,单质Y、Z生成B,则Y应为氮元素、X应为氧元素,则A为NO、B为H2O、C为NH3,验证符合转化关系。
A.X为氧,X元素位于VIA族,故A正确;
B.C为NH3,1 molC中含有3mol共价键,故B正确;
C.A为NO、C为NH3,A和C在一定条件下能发生氧化还原反应,6NO+4NH3![]() 5N2+6H2O,故C正确;
5N2+6H2O,故C正确;
D.Y应为氮元素最高+5价、X应为氧元素,一般不显正价,故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】A~E等几种烃分子的球棍模型如图所示,据此回答下列问题.

(1)D的分子式为________,A的二氯取代物有_______种,属于同系物的是_________(填字母)。
(2)有关有机物E的结构或性质的说法正确的是________(填字母)。
a.是碳碳双键和碳碳单键交替的结构
b.有毒、不溶于水、密度比水小
c.不能使酸性KMnO4溶液和溴的四氯化碳褪色
d.一定条件下能与氢气或氧气反应
(3)已知有机物C能与HCN反应,原理与其和H2O反应类似,请写出相关的化学反应方程式:_________________,反应类型_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列物质 ①NaCl晶体②液态SO2 ③纯醋酸 ④硫酸钡⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KNO3 ⑧NaOH溶液 ⑨氨水 请用以上物质的序号回答下列问题:
属于强电解质的是________; 属于弱电解质的是_______;在上述状态下能导电的物质是_________。
(2)化学平衡移动原理同样也适用于其它平衡,已知在氨水中存在下列平衡:NH3·H2O ![]() NH4++OH-
NH4++OH-
①向氨水中加入NH4Cl固体时,平衡____________移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同)。
②向氨水中加入MgCl2固体时,平衡_____移动,(填“向右”或“向左”), c(NH4+)____(填“增大”或“减小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ |
(1)表中最活泼的金属是___________,非金属性最强的元素是____________。(填写元素符号,下同)
(2)表中能形成两性氢氧化物的元素是_______________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应水化物反应的化学方程式:___________、___________。
(3)⑨最高价氧化物对应水化物的电子式______________。
(4)利用下图装置来验证同主族元素非金属性的变化规律:
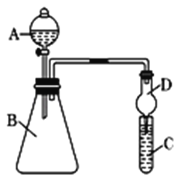
要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,应在B、D之间增加一个盛有足量____(选填下列字母:A 浓盐酸 、B 浓NaOH溶液、C 饱和Na2CO3溶液 、D 饱和NaHCO3溶液)的洗气装置.改进后C中发生反应的化学方程式是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种短周期主族元素,其中仅含有一种金属元素,A单质是自然界中密度最小的气体,A和D最外层电子数相同;C和B、E在周期表中均相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成A2C和A2C2两种常见的液态化合物.请回答下列问题:
(1)A元素的名称是____________,D在周期表中的位置____________,E的离子结构示意图____________。
(2)B2分子的电子式:____________,A2C的结构式:____________,A2C2中的化学键类型有:____________(极性键、非极性键或离子键)。
(3)用电子式表示D2E化合物的形成过程为______。
(4)用含A元素最简单的有机化合物与赤热的氧化铜反应生成一种单质、液态氧化物和一可以使澄清石灰水变浑浊的气体,其化学方程式为________。
(5)在100mL 18mol/L E的最高价氧化物对应水化物的溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解,产生的气体在标准状况下的体积可能是________(填序号)。
a 7.32L b 6.72L c 20.16L d 30.24L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基自由基(·OH,电中性,O 为-1 价)是一种活性含氧微粒。常温下,利用·OH 处理含苯酚废水,可将其转化为无毒的氧化物。
(1)·OH 的电子式为________。
(2) pH=3 时 Fe2+催化 H2O2 的分解过程中产生·OH 中间体,催化循环反应如下。将方程式 ii 补充完整。
i.Fe2++ H2O2+H+ = Fe3++ H2O +·OH
ii.___ + ___= ___+ O2↑+2H+
(3)已知:羟基自由基容易发生猝灭 2·OH = H2O2,从而活性降低.用 H2O2 分解产生的·OH 脱除苯酚,当其他条件不变时,不同温度下,苯酚的浓度随时间的变化如图 1 所示.0~20 min 时,温度从40℃上升到 50℃,反应速率基本不变的可能原因是________。
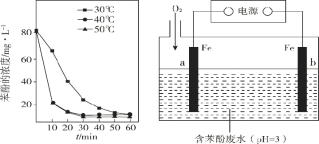
(4)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚废水更加高效,装置如图2所示。已知 a 极主要发生的反应是 O2 生成 H2O2,然后在电解液中产生·OH 并迅速与苯酚反应。
①b 极连接电源的________极(填“正”或“负”)。
②a 极的电极反应式为______。
③除电极反应外,电解液中主要发生的反应方程式有 ________ , _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)原子半径最小的元素是___(填元素名称),写出⑧的原子结构示意图____________。
(2)最高价氧化物对应的水化物中,碱性最强的是___(用化学式回答,下同),酸性最强的是____。
(3)①与⑤形成的化合物中,化学键类型为____。
(4)⑦与⑨形成的化合物的电子式为__,②与④形成的原子个数比为1:2的化合物的结构式为__。
(5)①与②形成的一种烃,具有平面正六边形结构,相对分子质量为78,写出此烃发生取代反应的化学方程式(任写一个即可):_。
(6)为探究元素②和⑧的非金属性强弱,某同学设计了如图所示的装置进行实验(夹持仪器已略去,装置气密性良好)。请回答:
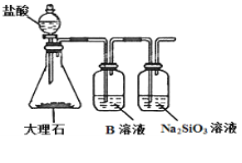
①溶液B为______,B溶液的作用是______。
②若看到_______现象,即可证明酸性_______(用化学式回答),则非金属性______(用元素符号回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海带中提取碘,可经过以下实验步骤完成。下列有关说法正确的是
![]()
A. 灼烧过程中使用的玻璃仪器有酒精灯、烧杯、玻璃棒
B. 氧化过程中发生反应的离子方程式为 2I-+H2O2 =I2+2OH-
C. 检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明海带中含有碘单质
D. 分液时,先打开活塞放出下层液体,再关闭活塞从上口倒出上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以AgZSM为催化剂,在容积为1L的容器中,相同时间下测得0.1molNO转化为N2的转化率随温度变化如图所示[无CO时反应为2NO(g)![]() N2(g)+O2(g);有CO时反应为2CO(g)+2NO(g)
N2(g)+O2(g);有CO时反应为2CO(g)+2NO(g)![]() 2CO2(g)+N2(g)]。下列说法错误的是( )
2CO2(g)+N2(g)]。下列说法错误的是( )
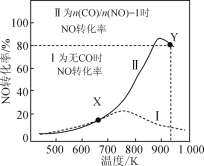
A.反应2NO![]() N2+O2的ΔH>0
N2+O2的ΔH>0
B.达平衡后,其他条件不变,使![]() >1,CO转化率下降
>1,CO转化率下降
C.X点可以通过更换高效催化剂提高NO的反应速率
D.Y点再通入CO、N2各0.01mol,此时v(CO,正)<v(CO,逆)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com