
【题目】请将符合题意的下列变化的序号填在对应的横线上:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解。
(1)化学键没有被破坏的是__________;仅发生离子键破坏的是__________;
(2)即发生离子键破坏、又发生共价键破坏的是____________________;
(3)N2的电子式为__________;Na2O2的电子式为___________;CO2的电子式为_________。
【答案】①② ③④ ⑥ ![]()
![]()
![]()
【解析】
根据过程中发生变化的特点以及是否有新物质生成、是否形成新化学键判断;根据物质中含有的化学键书写相应的电子式。
(1)①碘升华时,碘由固态转化为气态,只是物质状态发生变化,化学键不被破坏;
②氧气溶于水时,氧气分子存在于水中,化学键不被破坏;
③氯化钠溶于水时,氯化钠在水分子的作用力电离出钠离子和氯离子,离子键被破坏;
④烧碱熔化时,NaOH电离出钠离子和氢氧根离子,离子键被破坏;
⑤氯化氢溶于水,氯化氢在水分子的作用下电离出氢离子和氯离子,共价键被破坏;
⑥氯化铵受热分解生成氨气和氯化氢,离子键和共价键被破坏;
通过以上分析知,化学键没有被破坏的是①②;仅发生离子键破坏的是③④;
(2)既发生离子键又发生共价键破坏的是⑥;
(3)氮气为共价分子,氮氮原子间形成三对共用电子对,其电子式为![]() ;Na2O2为离子化合物,钠离子和过氧根离子间为离子键,其电子式为
;Na2O2为离子化合物,钠离子和过氧根离子间为离子键,其电子式为![]() ;CO2为共价化合物,碳氧原子间形成双键,其电子式为
;CO2为共价化合物,碳氧原子间形成双键,其电子式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“实验结论”与“实验操作及现象”相符的一组是
选项 | 实验操作及现象 | 实验结论 |
A | 向某溶液中加入 | 该溶液中一定含有 |
B | 向某溶液中加入稀盐酸,有无色气体产生 | 该溶液中一定含有 |
C | 向某溶液中加入 | 该溶液中一定含有 |
D | 向某溶液中加入酚酞溶液,溶液变为红色 | 该溶液中一定含有 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化工原料1,4-二苯基-1,3-丁二烯及某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
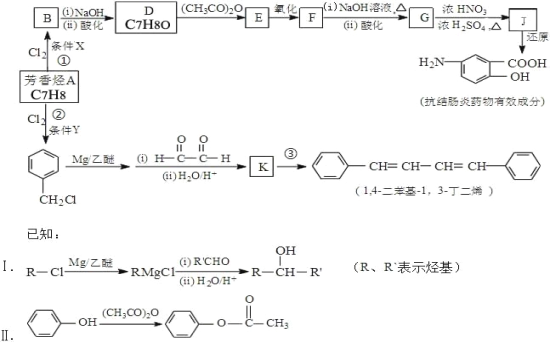
(1)抗结肠炎药物有效成分分子中的含氧官能团名称是________。
(2)②中的反应条件是________;G生成J的反应类型是________。
(3)①的化学方程式是________。
(4)F的结构简式是________。
(5)③的化学方程式是________。
(6)设计D→E和F→G两步反应的目的是________。
(7)1,4-二苯基-1,3-丁二烯有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:_________。
a.结构中有两个苯环,无其它环状结构 b.苯环上的一硝基取代产物有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,根据如图所示的实验装置,回答下列问题:
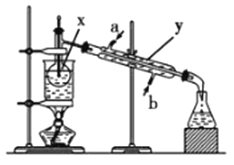
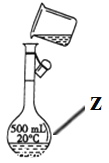
(1)写出下列仪器的名称:x_________;y_____________;z_____________。
(2)仪器y的进水口为_____________(填“a”或“b”)。
(3)请分别指出图中的一处错误_____________________,_________________。
(4)在配置1.0mol/L盐酸溶液时,下列操作会导致所配溶液浓度偏大的是___________(填写字母,下同);浓度不变的是_______。
A.用量筒量取浓盐酸时,俯视量筒刻度线
B.容量瓶未干燥即用来配置溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容后,将容量瓶倒置摇匀,发现液面低于刻度线,继续加水至刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
F.未进行洗涤操作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
CH3CH===CH2+CO+H2![]() CH3CH2CH2CHO
CH3CH2CH2CHO![]() 1-丁醇
1-丁醇
CO的制备原理:HCOOH![]() CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。
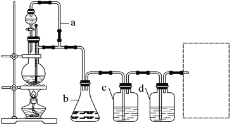
请填写下列空白:
(1)1-丁醇的结构简式:______,HCOOH的名称______,浓硫酸在制备CO中体现的性质有____(填“脱水性”、“吸水性”、“强氧化性”或“酸性”);
(2)若用图装置制备干燥纯净的CO,装置中a和b的作用分别是______,______;温度计的作用是_____________,分液漏斗、c和d中盛装的试剂分别是____,____,____。若用图装置制备H2,在虚线框内画出收集干燥H2的装置图______;
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂(试剂足量)检验这四种气体,混合气体通过试剂的顺序是____________(填序号);
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4 ⑤品红溶液
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是____________;
a.低温、高压、催化剂 b.适当的温度、高压、催化剂
c.常温、常压、催化剂 d.适当的温度、常压、催化剂
(5)正丁醛经催化加氢得到含少量正丁醛的1丁醇粗品。为纯化1丁醇,该小组查阅文献得知。①R—CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;②沸点:乙醚34 ℃,1丁醇118 ℃,并设计出如下提纯路线:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
操作1为_______________,操作2______________,若利用图1装置中已有的仪器实现操作3,还必须增加的实验仪器有______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com