
【题目】我国某地粉煤灰中镓含量丰富,其主要成分以Ga2O3的形式存在,除此之外还含有A12O3、Fe3O4、SiO2等杂质。已知从粉煤灰中回收镓的艺流程如图甲所示。
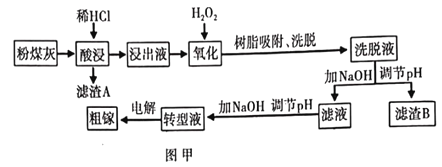
信息:(i)转型液中镓以GaO2-的形式存在;
(ii)Ksp[Ga(OH3)]=1.4×10-34,Ksp[Fe(OH)3]=2.7×10-39,Ksp[Fe(OH)2]=4.87×10-17。
回答下列问题:
(1)滤渣A中一定含有的成分是___________。
(2)“氧化”过程中加入H2O2的目的是___________,该过程中发生反应的离子方程式为___________。
(3)洗脱液中还有少量的Fe3+、Ga3+,其中Ga3+浓度为1.4×10-4mol/L,列式计算当Fe3+恰好沉淀完全时[c(Fe3+)≤1.0×10-5mol/L],G a3+是否开始沉淀___________。
(4)流程图中两次调节pH的目的分别是___________。
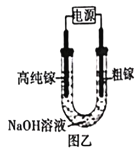
(5)电解法可以提纯粗镓,具体原理如图乙所示①粗镓与电源___________极相连(填“正”或“负”)。②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式为___________。
【答案】SiO2 将Fe2+氧化为Fe3+,便于后续操作分离 2Fe2++H2O2+2H+==2Fe3++2H2O 当Fe3+恰好沉淀时,溶液中c3(OH-)=Ksp[Fe(OH)3]/c(Fe3+)=2.7×10-39/1.0×10-5mol3/L3=2.7×10-34mol3/L3,Qc[Ga(OH)3]=c(Ga3+)c3(OH-)=1.4×10-4mol/L×2.7×10-34mol3/L3 =3.78×10-38<Ksp[Ga(OH)3],故Ga3+未开始沉淀 第一次调节pH是为了使Fe3+沉淀从而分离,第二次调节pH是为了将Ga3+转化为GaO2—得到转型液 正 GaO2—+3e—+2H2O==Ga+4OH—
【解析】
粉煤灰中主要成分Ga2O3,还含有A12O3、Fe3O4、SiO2等杂质,加入盐酸后,SiO2不反应,过滤留在滤渣A中,浸出液中的Fe2+被H2O2氧化,变成Fe3+,加氢氧化钠调节pH后,根据Ksp[Ga(OH3)]=1.4×10-34,Ksp[Fe(OH)3]=2.7×10-39,使Fe3+变成沉淀进行分离,第二次调节pH是为了将Ga3+转化为GaO2—得到转型液,GaO2—在阴极得电子,被还原为金属Ga。以此分析解答此题。
(1)结合上述分析滤渣A中一定含有的成分是SiO2。
(2)“氧化”过程中加入H2O2的目的是将Fe2+氧化为Fe3+,便于后续操作分离,该过程中发生反应的离子方程式为2Fe2++H2O2+2H+==2Fe3++2H2O。
(3)当Fe3+恰好沉淀时,溶液中c3(OH-)=Ksp[Fe(OH)3]/c(Fe3+)=2.7×10-39/1.0×10-5mol3/L3=2.7×10-34mol3/L3,Qc[Ga(OH)3]=c(Ga3+)c3(OH-)=1.4×10-4mol/L×2.7×10-34mol3/L3 =3.78×10-38<Ksp[Ga(OH)3],故Ga3+未开始沉淀。
(4) 第一次调节pH是为了使Fe3+沉淀从而分离,第二次调节pH是为了将Ga3+转化为GaO2—得到转型液;
(5)类比电解法精炼铜的原理可知,粗镓与电源正极相连,失电子,发生氧化反应,镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式为GaO2—+3e—+2H2O==Ga+4OH—。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】某离子反应涉及到H2O、ClO-、NH4+、OH-、N2、Cl- 几种微粒,其中N2、ClO- 的物质的量随时间变化的曲线如图所示。下列说法正确的是

A.该反应中Cl- 为氧化产物
B.消耗1mol还原剂,转移3mol电子
C.反应后溶液的碱性增强
D.该反应氧化剂与还原剂物质的量之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列情况会使所配溶液浓度偏低或其他测量值偏低的是( )
①用稀醋酸和稀氢氧化钠溶液反应测定中和热数值;②用滴定管量取液体时,开始时平视读数,结束时俯视读数所得溶液的体积;③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤;④在用标准液(已知浓度)滴定未知溶液时,盛标准液的滴定管水洗后未润洗;⑤定容时,仰视容量瓶的刻度线
A. ①③⑤B. ①②⑤
C. ②③④D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物的绿色细胞在光照下吸收O2、释放CO2的现象,称为光呼吸。研究发现,光呼吸是光照条件下O2/CO2的值异常时发生的一种生理过程,光呼吸和光合作用暗反应的关系如图所示。请回答下列有关问题:
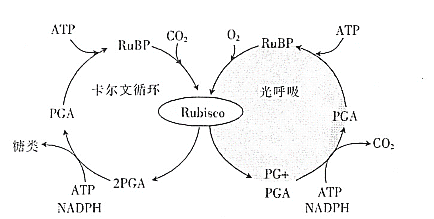
注:RuBP为1,5-二磷酸核酮糖,是卡尔文循环里起重要作用的一种五碳糖;PGA为三磷酸甘油酸,是一种三碳化合物;PG为二碳化合物;Rubisco为1,5-二磷酸核酮糖羧化酶/加氧酶。
(1)植物的卡尔文循环中,RuBP结合CO2的过程发生在_______________(填场所)中,图中卡尔文循环和光呼吸均利用的物质有_______________。结合上图,请从O2和CO2含量的角度分析,光照条件下光呼吸进行的条件是_______________。
(2)光呼吸的最终产物是_______________,这个过程是_______________(填“产生”或“消耗”)能量的过程。
(3)根据图中光呼吸与光合作用暗反应的关系推测,抑制光呼吸对农作物生产的意义是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在绿色植物体内存在一种RUBP羧化酶。该酶在CO2浓度较高时,催化C5与CO2反应,生成C3化合物;在O2浓度较高时,催化C5与O2反应,部分产物经一系列变化后转移到线粒体中会产生CO2,我们把这一过程又称为光呼吸(如图所示)。

光呼吸会消耗光合作用过程中新形成的有机物,还能消耗细胞内过多的ATP和还原剂[H],以防止它们的积累影响细胞的正常代谢。为了与光呼吸相区别,研究人员把细胞通常进行的呼吸成为“暗呼吸”。请回答:
(1)RUBP羧化酶的存在场所为_____________________,它的催化作用机理是____________________。
(2)在较高CO2浓度环境中,RUBP羧化酶所催化反应的产物是C3,该产物的还原还需要光反应提供_______________。
(3)光呼吸会降低农作物产量,但是在长期进化过程中却被保留下来,那么光呼吸存在的意义可能是________________、_____________________等。
(4)夏季中午,水稻出现“光合午休”现象,有机物的积累速率明显下降,其原因可能是因为叶片气孔的大量关闭使CO2浓度下降进而导致______________________________________________________。(从两个方面回答)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是
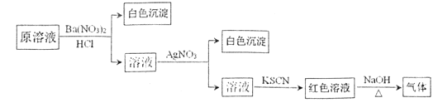
A.原溶液中一定含有![]() 离子B.原溶液中一定含有
离子B.原溶液中一定含有![]()
C.原溶液中一定含有Cl-离子D.原溶液中一定含有Fe3+离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为M的气态化合物VL(标准状况)溶于mg水中,得到溶液的质量分数为ω%,物质的量浓度cmol/L,密度为ρg/cm3,则下列说法正确的是
A. 相对分子质量M可表示为:![]()
B. 溶液密度ρ可表示为:![]()
C. 溶液的质量分数ω%可表示为:![]()
D. 物质的量浓度C可表示为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法合理的是
①根据纯净物中是否含氧元素,来判断是否属于氧化物
②根据电泳现象可证明胶体带电荷
③直径介于lnm~l00nm之间的微粒称为胶体
④金属氧化物都是碱性氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液
⑥同一钢笔使用不同牌号的墨水容易堵塞,是由于胶体的聚沉
A. 只有⑥ B. 只有②⑥ C. 只有③④⑤ D. 只有①②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B的结构简式如下:

(1)A分子中含有的官能团的名称是____________________________________。
(2)A、B能否与NaOH溶液反应:A________(填“能”或“不能”,下同),B________。
(3)A在浓硫酸作用下加热可得到B,其反应类型是____________________。
(4)A、B各1 mol分别加入足量溴水,完全反应后消耗单质溴的物质的量分别是________mol、________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com