



 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
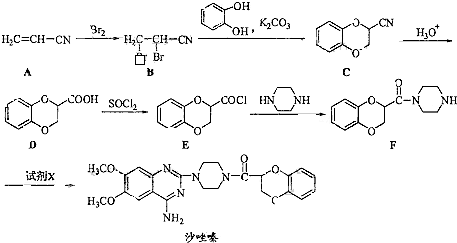
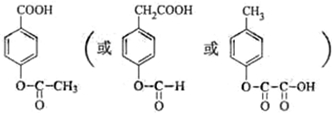

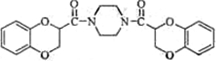

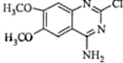

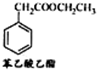
| ||
| 170℃ |
| Br2 |
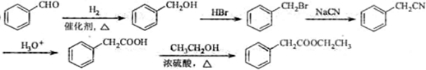

查看答案和解析>>
科目:高中化学 来源: 题型:
2009年度江苏省级节能减排(节能与循环经济)专项引导资金实施公交车“油改气”工程。公交车印有“CNG”标志(CNG汽车是指以压缩天然气替代常规汽油或柴油作为汽车燃料的汽车)。城市推行这一改革的主要目的是( )

A.延长发动机的寿命 B.促进地方经济的发展,增加再就业机会
C.节约能源 D.减少大气污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com