
【题目】下列措施符合“绿色化学”思想的是
A. 直接排放含磷生活污水
B. 大量使用氟里昂作为冰箱制冷剂
C. 使用可降解塑料代替不可降解塑料
D. 使用化学性质稳定、不易分解的有机氯农药
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】如表物质与其所含化学键类型、所属化合物类型完全正确的一组是( )
选项 | A | B | C | D |
物质 | CaCl2 | H2O2 | AlCl3 | NH4Cl |
所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键、共价键 |
所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 共价化合物 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、M 均为短周期元素。25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol/L)溶液的pH和原子半径的关系如图所示。下列说法不正确的是

A. X、M 简单离子半径大小顺序:X>M
B. X、Y、Z、W、M 五种元素中只有一种是金属元素
C. Z 的最高价氧化物的化学式为ZO3
D. X、Z的最简单气态氢化物反应现象:有白烟生成XY ZW
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和.
(1)C离子的结构示意图为 . D在周期表中位置.
(2)A、D两元素形成的化合物属(填“离子”或“共价”)化合物.
(3)写出E的电子式: .
(4)写出D的最高价氧化物的水化物和A反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是以实验为基础的.利用已学知识对下列实验进行分析并填空:
Ⅰ.某研究性学习小组设计了一组实验来探究元素周期律.
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置完成同主族元素C、Si非金属性强弱比较的实验研究;
乙同学设计了如图2装置实验来验证卤族元素性质的递变规律(夹持装置已略去).A、B、C三个胶头滴管分别是氯酸钾溶液、NaBr溶液、淀粉KI溶液.已知常温下浓盐酸与氯酸钾溶液能反应生成氯气.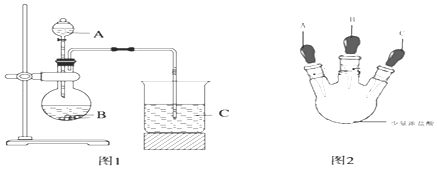
(1)甲同学设计实验所涉及的离子方程为:、 .
(2)乙同学具体操作如下:
①先挤压胶头滴管A,使少量溶液滴入烧瓶内;
②挤压胶头滴管B,使稍过量溶液滴入烧瓶内,充分反应.写出该操作中主要离子方程式为 .
③再挤压胶头滴管C,使少量溶液滴入烧瓶内,可观察到;
(3)根据甲乙同学的实验可得到的结论是:
(4)II.
实验 |
| ||
实验 |
|
|
|
实验 | 结论: | ||
反应 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X和Y的离子X2+和Y2-具有相同的电子层结构,则下列说法正确的是
A. X2+的离子半径比Y2-小 B. X2+的原子序数比Y2-小
C. X和Y原子的电子层数相等 D. X和Y原子最外层电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解气主要含有丙烯、1,3-丁二烯等不饱和烃,以它们为原料可合成CR橡胶和医药中间体G,,合成路线如下:

已知:①B、C、D 均能发生银镜反应;
②
(1)A的顺式异构体的结构简式为___________________。
(2)C中含氧官能团的名称是____________,反应①的反应类型为____________________。
(3)写出E→ 反应的化学方程式:_________________________________。
(4)写出同时满足下列条件的医药中间体G的同分异构体的结构简式: __________________。
①与D 互为同系物; ②核磁共振氢谱有三组峰。
(5)用简要语言表述检验B中所含官能团的实验方法:_______________________。
(6)以A为起始原料合成CR橡胶的线路为______________________(其它试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大.已知在周期表中A是原子半径最小的元素,B的气态氢化物能与其最高价氧化物的水化物反应,C原子最外层电子数是电子层数的3倍,D+和E3+离子的电子层结构相同,C与F属于同一主族.请回答下列问题:
(1)F在元素周期表中的位置是________________。
(2)上述B、C、D、E、F、G元素形成的简单离子中,半径最小的是_______(填离子符号)。
(3)由上述元素中的一种或几种组成的物质甲可以发生如图反应:
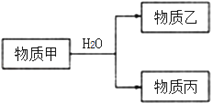
①若乙具有漂白性,则乙的电子式为________。
②若丙的水溶液是强碱性溶液,则甲为________________(填化学式)。
(4)G和F两种元素相比较,非金属性较强的是(填元素名称)________,可以验证该结论的是________(填写编号)。
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的含氧酸的酸性
(5)A、B两种元素形成一种离子化和物,该化合物所有原子最外层都符合相应稀有气体原子最外层电子结构则该化合物电子式为________________。
(6)由A、B、C、F、四种元素组成的一种离子化合物X,已知:① 1 mol X能与足量NaOH浓溶液反应生成标准状况下22.4 L气体;② X能与盐酸反应产生气体Y,该气体能与氯水反应,则X是________________(填化学式),写出该气体Y与氯水反应的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下(T2>T1),在3个体积均为2.0L的恒容密闭容器中反应2NO(g)+Cl2(g)=2ClNO(g) (正反应放热)达到平衡,下列说法正确的是
容器 | 温度/ (℃) | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/ mol·L-1 | ||
c(NO) | c(Cl2) | C(ClNO).v | C(ClNO) | ||
Ⅰ | T1 | 0.20 | 0.10 | 0 | 0.04 |
Ⅱ | T2 | .020 | 0.10 | 0.20 | cl |
Ⅲ | T3 | 0 | 0 | 0.20 | C2 |
A. 达到平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为1:2
B. 达到平衡时,容器Ⅲ中ClNO的转化率小于80%
C. 达到平衡时,容器Ⅱ中c(ClNO)/C(NO)比容器Ⅰ中的大
D. 若温度为T1,起始时向同体积恒容密闭容器中充入0.20molNO(g).、0.2mo1Cl2(g)和0.20molClNO(g),则该反应向正反应方向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com