
【题目】下列反应的离子方程式书写正确的是
A. 金属铝溶于稀硫酸中:Al+2H+=Al3++H2↑
B. 铜片溶于稀硝酸产生无色气体:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
C. 向NaClO溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3-
D. 用惰性电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+4H++O2↑
2Cu+4H++O2↑
 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】过氧化尿素是一种新型漂泊、消毒剂,广泛应用与农业、医药、日用化工等领域。用低浓度的双氧水和饱和尿素溶液在一定条件下可以合成过氧化尿素。反应的方程式为:
CO(NH2)2+H2O2![]() CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
合成过氧化尿素的流程及反应装置图如图:

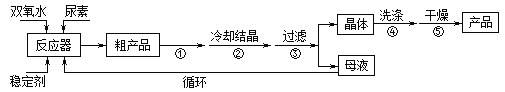
请回答下列问题:
(1)仪器X的名称是__________;冷凝管中冷却水从____(填“a”或“b”)口出来;
(2)该反应的温度控制30℃而不能过高的原因是_______________________。
(3)步骤①宜采用的操作是_____________。
A.加热蒸发 B.常压蒸发 C.减压蒸发
(4)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是_________________。
(5)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol·L﹣1H2SO4,用0.2000mol·L﹣1KMnO4标准溶液滴定至终点时消耗18.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2·H2O2的质量分数为_____________;若滴定后俯视读数,则测得的过氧化尿素含量________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质、用途的说法都正确的是
A. 硅晶体是良好的半导体,可用于制造光导纤维
B. 高压钠灯发出的黄光透雾能力强,可用于道路和广场照明
C. 生石灰能与水反应,可用于除去CO2气体中少量的水蒸气
D. 碳酸钠具有碱性,可用于治胃酸中和剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,第一种是电解质,第二种是分散系,第三种是合金的是 ( )
A. 硫酸、CuSO4·5H2O、生铁 B. 酒精、空气、铜绿
C. 二氧化碳、明矾、熟石灰 D. 硝酸钾、食盐水、黄铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神舟七号”的燃料是氢化锂三兄弟:LiH、LiD、LiT。其中Li的质量数为7,则对相同物质的量的这三种物质的下列说法正确的是( )
A. 质子数之比为1:2:3 B. 中子数之比为1:1:1
C. 摩尔质量之比为8:9:10 D. 化学性质不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)又称水合联氨,其纯净物为无色透明的油状液体,具有强碱性和吸湿性。将水合肼通入CuO胶体中,可发生如图所示的转化。

(1)图示的转化中,②属于_____________(填“非氧化还原反应”或“氧化还原反应”)。
(2)转化①中,氧化剂与还原剂的物质的量之比为4: l ,则X的化学式为_____。
(3)转化②中,反应一段时间后,溶液中n(OH-)____________(填“增大”“ 减小” 或“不变”)。
(4)若①中参加反应的CuO物质的量为0.4mol,按图示转化过程进行后,④中生成的CuO物质的量也等于0.4mol,则③中参加反应的O2的物质的量与④中今加反应的NaClO的物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的用途不合理的是
A. SiO2可用于制造光导纤维 B. 活性炭可用作除味剂
C. 浓硫酸可用于干燥碱性物质 D. NH4Cl可用作氮肥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是重要的非金属元素,可以形成多种化合物。回答以下问题:
(1)基态氮原子的电子排布式是________________。C、N、O三种元素第一电离能从大到小的顺序是____________________。
(2)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是________________________;N2H4分子中氮原子轨道的杂化类型是____________________。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(1)+2N2H4(1)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若该反应中有4molN-H键断裂,则形成的π键有_________mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__________(填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
(3)(CH3)3NH+和AlCl4-形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂___________(填“大”或“小”),可用作____________(填代号)。
a.助燃剂 b.“绿色”溶剂
c.复合材料 d.绝热材料
(4)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的元素符号是___________,与同一个N3-相连的X+有_________个。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com