
【题目】在25℃时,用蒸馏水稀释1 mol·L-1氨水至0.01 mol·L-1,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A. ![]() B.
B. ![]() C.
C. ![]() D. c(OH-)
D. c(OH-)
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)将纯锌片和纯铜片按下图方式插入相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法中正确的是(填序号).
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中H+的浓度均减小
②在相同时间内,两烧杯中产生气泡的速率:甲乙(填“>”、“<”或“=”).
③甲中硫酸根离子向极移动(填“铜”或“锌”)
④当甲中产生1.12L(标准状况)气体时,理论上通过导线的电子数目为 .
(2)欲将反应2Fe3++Cu═Cu2++2Fe2+设计成原电池,该电池负极材料为 , 电解质溶液为 , 正极反应为 , 10min内该电池向外提供0.1mol电子,则正极材料与负极材料的质量差为g(假设刚开始时,两电极的质量相等).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:3X(气)+Y(气)=nZ(气)+2W(气).5min末已生成0.2molW,若测知以Z浓度变化来表示的化学反应平均速率为0.01molL﹣1min﹣1 , 则上述反应中Z气体的计量系数 n的值是( )
A.1
B.2
C.3
D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1molL﹣1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法不正确的是( ) 
A.OP段发生的反应为:OH﹣+H+═H2O
B.图中V2为100
C.沉淀的质量m为1.56 g
D.原合金质量为0.92 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W相邻;
②X分别与Y、Z、W可组成化学式为YX3 , X2Z和X2W三种共价化合物
请填空:
(1)X、Y、Z原子最外层电子数之和是
(2)X2W的结构式是
(3)X、Y和Z组成的一种化合物是强酸.写出该酸的稀溶液与铜反应的离子方程式含Y、Z的气体和一种只含X、Z的液体(在常温、常压下)反应可以生成一种离子化合物其化学式为
(4)X、Y、Z和W组成一种化合物,其原子个数之比为5:1:3:1;该化合物具有还原性.①写出该化合物与过量稀NaOH溶液反应的离子方程式: .
②请设计实验证明该化合物具有还原性: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 化学电池的放电过程就是电能转换为化学能的过程
B. 化学电池中电子由正极流出,经外电路流向负极
C. 物质燃烧总是放热的,燃料电池两极板均发生氧化还原反应
D. 燃料电池工作时,通常是将空气通向正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时,某化学实验小组同学向用大理石和稀盐酸制备CO2后的残留液中滴加碳酸钠溶液,在溶液中插入pH传感器,测得pH变化曲线如图所示.下列说法不正确的是( ) 
A.开始时溶液pH=2是因为残留液中还有盐酸剩余
B.BC段表示随着碳酸钠溶液的滴入,CaCO3沉淀的质量逐渐增加
C.滴入500滴碳酸钠溶液后溶液中c(OH﹣)>c(H+)
D.AB发生的反应为:Ca2++CO32﹣═CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过下述流程回收Na2Cr2O7等物质. 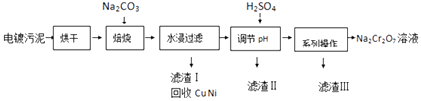
已知:
①Cr(OH)3、ZnO和Al2O3一样均为两性化合物;
②Na2Cr2O7、Na2SO4在不同温度下的溶解度如表:
20℃ | 60℃ | 100℃ | |
Na2SO4 | 19.5 | 45.3 | 42.5 |
Na2Cr2O7 | 183 | 269 | 415 |
(1)焙烧过程中生成Na2CrO4的化学方程式为;水浸后溶液中除Na2CrO4还存在的溶质有和;
(2)加入H2SO4调节pH的目的为;
(3)得到滤渣Ⅲ的“系列操作”的步骤为、过滤;
(4)若1L加入H2SO4后所得溶液中含铬元素质量为23.4g,CrO42﹣有8/9转化为Cr2O72﹣ , 求转化后所得溶液中c(Cr2O72﹣)=molL﹣1;
(5)向Na2Cr2O7与H2SO4混合液中加入H2O2 , 再加入乙醚并摇动,乙醚层为蓝色.乙醚中溶有CrO5 , 则发生反应的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com