
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
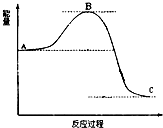 已知2SO2(g)+O2(g)
已知2SO2(g)+O2(g) | 加热 |
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
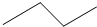

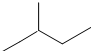

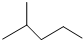
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲苯与硝酸制TNT |
| B、乙烯聚合为聚乙烯高分子材料 |
| C、溴乙烷水解制乙醇 |
| D、甲烷与氯气制备一氯甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
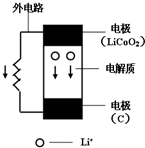 某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6
某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6| 充电 |
| 放电 |
| A、外电路上的“→”表示放电时的电流方向 |
| B、充电时阴极电极反应:LixC6-xe-═6C+xLi+ |
| C、放电时负极电极反应:LiCoO2-xe-═Li1-xCoO2+xLi+ |
| D、外电路有0.1mol e-通过,发生迁移的Li+的质量为0.7g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com