
| A.1mol/L Na2CO3溶液中的Na+ 数目为2NA |
| B.标准状况下,11.2LSO3所含分子数为0.5NA |
| C.1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA电子 |
| D.各5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA |
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源:不详 题型:单选题
| A.阿伏加德罗常数就是指6.02×1023 |
| B.1 mol 任何物质都约含有6.02×1023个分子 |
| C.3.01×1023个Na+的物质的量是0.5 mol |
| D.2 mol SO42-约含有1.204×1023个SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温常压下,11.2 L甲烷中含有的氢原子数为2NA |
| B.标准状况下,0.3 mol二氧化碳中含有氧原子数为0.3 NA |
| C.常温下,2.7 g铝与足量的盐酸反应,失去的电子数0.3 NA |
| D.常温下,1 L 0.1 mol / L MgCl2溶液中含Mg2+数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 L 0.1 mol·L-1的CuCl2溶液中含Cu2+为0.1NA |
| B.标准状况下,22.4 L CCl4含CCl4分子为NA |
| C.1mol H3O+含质子数为10 NA |
| D.1molNa2O和Na2O2混合物中含阴离子的总数为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化碳的相对分子质量是44 | B.“物质的量浓度”可简称为“量浓度” |
| C.阿伏加德罗常数的单位是mol-1 | D.1 mol任何物质所占体积都是22.4 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol?L-1 | B.0.5 mol?L-1 | C.0.25 mol?L-1 | D.0.2 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
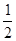 H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。
H2O)、无水石膏(CaSO4)三种成分组成,各组分含量可用下列方法测定。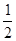 H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。
H2O,此时,其它两组分与酒精溶液不起作用;将试样取出干燥后称量,试样质量变为8.97 g。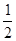 H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。
H2O都水化成CaSO4·2H2O,取出干燥后再次称量,质量变为10.32 g。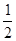 H2O)∶n(CaSO4)= __________________。
H2O)∶n(CaSO4)= __________________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com