
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)⇌CuS(s)+Mn2+(aq),下列说法错误的是()
A. 相同条件下,MnS的Ksp比CuS的Ksp大
B. 该反应的平衡常数K=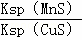
C. 该反应达到平衡时c(Mn2+)=c(Cu2+)
D. 往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
考点: 难溶电解质的溶解平衡及沉淀转化的本质.
专题: 电离平衡与溶液的pH专题.
分析: A.根据分子式相似的分子,溶度积大的沉淀可以转化为溶度积小的沉淀;
B.反应的平衡常数K=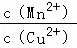 =
=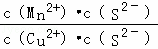 =
=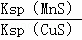 ;
;
C.该反应达到平衡时离子的浓度不变;
D.增大铜离子的浓度平衡正移.
解答: 解:A.分子式相似的分子,溶度积大的沉淀可以转化为溶度积小的沉淀,所以MnS的Ksp比CuS的Ksp大,故A正确;
B.反应的平衡常数K=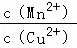 =
=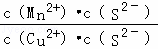 =
=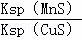 ,故B正确;
,故B正确;
C.该反应达到平衡时各离子的浓度保持不变,但不一定相等,故C错误;
D.增大铜离子的浓度,平衡正向移动,所以C(Mn2+)变大,故D正确;
故选C.
点评: 本题主要考查了沉淀的平衡以及转化,难度不大,根据平衡移动原理以及沉淀转化的知识即可完成.


 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
能说明醋酸是弱电解质的事实是()
A. 醋酸水溶液能使湿润的蓝色石蕊试纸变红
B. 醋酸和碳酸钠溶液反应放出二氧化碳
C. c(H+)相同的醋酸和盐酸相比较,醋酸溶液的浓度大
D. 浓度和体积均相同的醋酸和盐酸可中和等物质的量的NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的装置,C、D、E、F均为惰性电极.将电源接通后,向乙中滴入酚酞溶液,在F极附近显红色.试回答下列问题:(1)电极A是正极填“正极”或“负极”)
(2)甲装置中C极的电极反应式为.
(3)若用惰性电极电解饱和NaCl溶液一段时间,当阳极产生56 mL(标准状况下)气体,电解后溶液体积为500 mL时,所得溶液在25℃时的pH=.
(4)欲用丙装置给铜镀银,G应该是银(填“铜”或“银”),电镀液的主要成分是(填化学式).

查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验所对应的离子方程式正确的是()
A. 向NaAlO2溶液中通入少量CO2:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣
B. 向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+
C. 在碳酸氢钡溶液中加入过量的氢氧化钠溶液:Ba2++2HCO3﹣+2OH﹣═BaCO3↓+CO32﹣+2H2O
D. 向FeCl2溶液中加入少量K3[Fe(CN)6]溶液:4Fe2++2[Fe(CN)6]4﹣═Fe4[Fe(CN)6]2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或记录正确的是 ( )
A.用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g
B.用量筒测得排水法收集制得的氢气体积为50.28 mL
C.用两只250 mL的容量瓶配制0.1 mol·L-1500 mLNaOH溶液
D.常温常压下测得1 mol N2的质量为28 g
查看答案和解析>>
科目:高中化学 来源: 题型:
在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是 ( )
A.反应混合物的浓度 B. 反应体系的压强
C.正、逆反应的速率 D. 反应物的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的系统命名中,错误的是( )
A.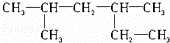
2,4﹣二甲基己烷
B.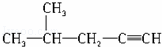
2﹣甲基﹣4﹣戊炔
C.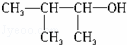
3﹣甲基﹣2﹣丁醇
D.CH3﹣CHBr﹣CHBr﹣CH3 2,3﹣二溴丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上部分内容.据此下列说法正确的是()

A. 该试剂的物质的量浓度为9.2 mol•L﹣1
B. 该硫酸50 mL与足量的铜反应可得到标准状况下SO2 10.3 L
C. 配制200 mL 4.6 mol•L﹣1的稀硫酸需取该硫酸50 mL
D. 该硫酸与等体积的水混合所得溶液的质量分数小于49%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com