
| A.SO3与水 | B.SO2与水 | C.SO2与氯水 | D.SO3与NaOH溶液 |
科目:高中化学 来源:不详 题型:填空题
| A.高沸点 | B.强酸性 | C.吸水性 | D.脱水性E.强氧化性F.催化作用(填序号) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 方法I | 用氨水将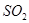 转化为 转化为 ,再氧化成 ,再氧化成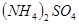 。 。 |
| 方法II | 用生物质热结气(主要成分: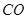 、 、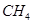 、 、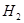 )将 )将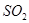 在高温下还原成单质硫 在高温下还原成单质硫 |
| 方法III | 用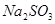 溶液吸收 溶液吸收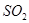 ,再经电解转化为 ,再经电解转化为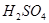 。 。 |
 易溶于水的
易溶于水的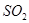 所形成的溶液中存在着下列平衡:
所形成的溶液中存在着下列平衡:
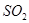 分子
分子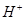 浓度是
浓度是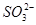 浓度的2倍
浓度的2倍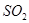 气体
气体 量
量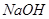 可得到
可得到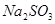 、
、 的混合溶液
的混合溶液 吸收燃煤烟气中
吸收燃煤烟气中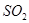 的离子方程式为______________。能提高燃煤烟气中
的离子方程式为______________。能提高燃煤烟气中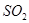 去除率的措施有______________(填字母)
去除率的措施有______________(填字母)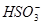 转化为
转化为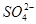
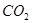 ,原因是(用离子方程式表示)________________________________________________________。
,原因是(用离子方程式表示)________________________________________________________。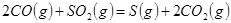
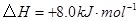

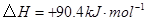
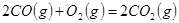

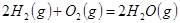
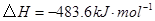
 反应生成
反应生成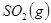 的热化学方程式为___________________。
的热化学方程式为___________________。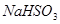 溶液的装置如下图所示(阴离子交换膜只允许阴离子通过)。阳极区放出的气体的成分为_____________(填化学式)。
溶液的装置如下图所示(阴离子交换膜只允许阴离子通过)。阳极区放出的气体的成分为_____________(填化学式)。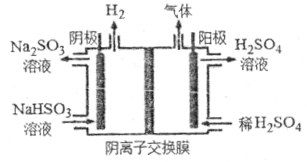
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
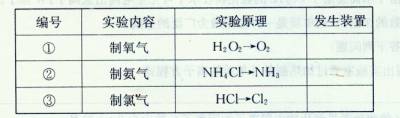
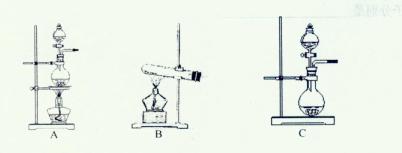
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com