
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
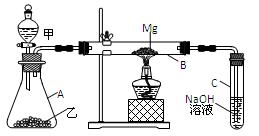
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. SO2具有漂白性,能使FeCl3、KMnOpK溶液迅速褪色 |
| B.可以用品红溶液鉴别SO2和CO2 |
| C.硫粉在过馈的纯氧中燃烧可以生成SO3 |
| D. SO2有漂白性,Cl2也有漂白性,两者同吋使用效果会更好 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
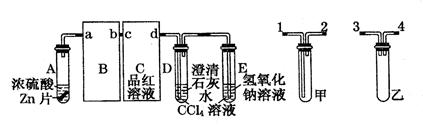
 为
为 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8 n1 =n2 | B.n1 =8n2 | C.n1 =n2 | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 贝尔化学奖授予致力于研究臭氧层被破坏问题的三位化学家。大气中的臭氧层可滤除大量的紫外线,保护地球上的生物。氟里昂(如 CCl2F2)可在光的作用下分解,产生C1原子。Cl原子会对臭氧层产生长久的破坏作用。有关反应为:
贝尔化学奖授予致力于研究臭氧层被破坏问题的三位化学家。大气中的臭氧层可滤除大量的紫外线,保护地球上的生物。氟里昂(如 CCl2F2)可在光的作用下分解,产生C1原子。Cl原子会对臭氧层产生长久的破坏作用。有关反应为: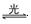 O2+O C1+O3→C1O+O2 ClO+O→C1+O2 总反应:2O3
O2+O C1+O3→C1O+O2 ClO+O→C1+O2 总反应:2O3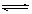 3O2
3O2| A.反应物 | B.生成物 | C.中间产物 | D.催化剂 |
| A.同分异构体 | B.同种物质 | C.氧的同素异形体 | D.氧的同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com