
【题目】请阅读下列材料,回答下列小题,
人们曾认为N+3H![]() 2NH化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化制,温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥。道解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
2NH化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化制,温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥。道解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
(1)合成氨的反应属于___________
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(2)下列反应条件的改变对反应速率的影响正确的是___________
A.增大N2的浓度能加快反应速率 B.减小H2的浓度能加快反应速率
C.升高温度能减慢反应速率 D.添加催化剂对反应速率无影响
(3)合成氨为放热反应,下列说法正确的是___________
A.断开H-H键放出能量
B.形成N-H键吸收能量
C.反应物的总能量大于生成物的总能量
D.反应物的总能量小于生成物的总能量
【答案】A A C
【解析】
根据各种不同类型反应特点判断反应类型;根据影响反应速率的条件分析判断;化学反应过程就是断裂反应物的化学键吸收能量与形成生成物化学键释放能量的过程分析。
(1)该反应的反应物是两种,生成物是一种,符合化合反应的含义,故合理选项是A;
(2)A.N2是气体反应物,增大反应物N2的浓度,化学反应速率加快,A符合题意;
B.减小气体反应物H2的浓度,化学反应速率减慢,B不符合题意;
C.在其它条件不变时,升高温度能加快化学反应速率,C不符合题意;
D.添加催化剂能加快化学反应速率,D不符合题意;
故合理选项是A;
(3) A.断开H-H键吸收能量,A错误;
B.形成N-H键放出能量,B错误;
C.该反应为放热反应,说明反应物的总能量大于生成物的总能量,C正确;
D.该反应为放热反应,说明反应物的总能量大于生成物的总能量,D错误;
故合理选项是C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,在体积固定的密闭容器中进行:N2(g)+3H2(g)![]() 2NH3(g),下列有关说法错误的是( )
2NH3(g),下列有关说法错误的是( )
A.达平衡时单位时间内生成氢气的物质的量与生成氨气的物质的量相同
B.使用催化剂可以加快反应速率,缩短达平衡时间
C.为了提高氢气的转化率,可以适当补充氮气
D.达平衡时,密闭容器中的气体的总物质的量比起始时的总物质的量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用酸性蚀刻废液(含![]() 等)和碱性蚀刻废液[NH4+、Cu(NH3)42+ 、NH3·H2O等]制备CuI(白色固体)的实验流程如下:
等)和碱性蚀刻废液[NH4+、Cu(NH3)42+ 、NH3·H2O等]制备CuI(白色固体)的实验流程如下:
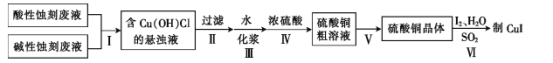
(1)步骤Ⅰ中发生了多个反应,其中![]() 与盐酸反应生成Cu(OH)Cl的离子方程式为____。
与盐酸反应生成Cu(OH)Cl的离子方程式为____。
(2)步骤Ⅳ需控制pH为1~2,80 ℃下进行,合适的加热方式是____。
(3)步骤Ⅴ的具体步骤是蒸发浓缩、______、____。
(4)步骤Ⅵ在下列装置(夹持及加热装置已省略)中进行。

①装置a中盛装浓硫酸的仪器的名称是___,圆底烧瓶中发生反应的化学方程式为___。
②装置c中反应完成的现象是_____。
③用装置d中的溶液洗涤制得的CuI的目的是____,然后再用无水乙醇洗涤的目的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素R、X、Y、Z。若它们的最外层电子数用n表示,则有:n(X)+n(Y)=n(Z),n(X)+n(Z)=n(R)。这四种元素组成一种化合物Q,Q具有下列性质:
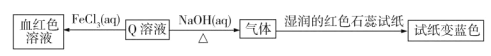
下列说法错误的是
A.原子半径:Y>Z>XB.最高价氧化物对应水化物酸性:Y<Z
C.X和Y组成的化合物在常温下都呈气态D.Y3Z4是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是
A. ![]() B.
B. ![]() C. n=m+17Vc D.
C. n=m+17Vc D. ![]() m<p<
m<p<![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①正丁醇沸点:117. 2℃,正丁醛沸点:75. 7℃;②CH3CH2CH2CH2OH![]() CH3CH2CH2CHO。利用如图装置用正丁醇合成正丁醛,下列说法不正确的是
CH3CH2CH2CHO。利用如图装置用正丁醇合成正丁醛,下列说法不正确的是

A.为防止产物进一步氧化,应将适量Na2Cr2O7酸性溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时收集产物
C.向分馏出的馏出物中加入少量金属钠,可检验其中是否含有正丁醇
D.向分离所得的粗正丁醛中,加入CaCl2固体,过滤,蒸馏,可提纯正丁醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理,实验时关闭图1中的a,用单孔塞(插有吸入水的胶头滴管)塞紧颈口c,将水挤入三颈烧瓶中,打开b,完成喷泉实验。电脑绘制三颈烧瓶内压强变化曲线图2。下列说法正确的是
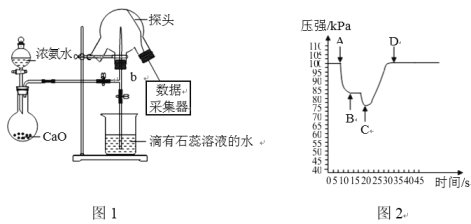
A.干燥氨气通常可选用浓硫酸B.三颈烧瓶内可以看到红色喷泉
C.由图2可知C点时喷泉最剧烈D.图1中氧化钙可用氯化钙代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种白色晶体,能潮解,难溶于水,可与水缓慢反应,不溶于乙醇,易与酸反应,常用作杀菌剂、防腐剂等。根据题意,回答相关问题。
I.CaO2晶体的制备:
CaO2晶体通常可利用CaCl2在碱性条件下与H2O2反应制得。某化学兴趣小组在实验室制备CaO2的实验方案和装置示意图如下:

(1)三颈烧瓶中发生的主要反应的化学方程式为_____。
(2)冷水浴的目的是____;步骤③中洗涤CaO2·8H2O的实验操作方法是______
Ⅱ.CaO2含量的测定:
测定CaO2样品纯度的方法是:称取0.200g样品于锥形瓶中,加入50mL水和15mL2mol·L-lHCl,振荡使样品溶解生成过氧化氢,再加入几滴MnCl2稀溶液,立即用0.0200mol·L-lKMnO4标准溶液滴定到终点,消耗25.00mL标准液。
(3)上述过程中使用稀盐酸而不使用稀硫酸溶解样品的原因是___ ;滴定前加入MnCl2稀溶液的作用可能是____。
(4)滴定过程中的离子方程式为_______,样品中CaO2的质量分数为______ 。
(5)实验I制得的晶体样品中CaO2含量偏低的可能原因是:①____;② ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气有毒,且大量制取的难度较大、污染严重,在培养皿中研究氯气的性质可实现“绿色实验”。在培养皿的点滴板中央孔穴中滴加能生成氯气的试剂(如漂粉精与盐酸),然后分别滴加所要进行实验的试剂,如下图。下列是某学生观察到的现象、解释与结论,其中不符合事实的是( )
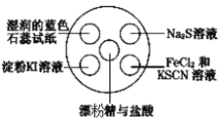
选项 | 实验现象 | 解释 | 结论 |
A | 淀粉 | 氯气置换出 | 氧化性: |
B |
| 氯气置换出 | 非金属性: |
C | 湿润的蓝色石蕊试纸先变红后褪色 | 氯气与水反应生成盐酸和次氯酸 | 氯气具有漂白性 |
D |
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com