
【题目】一种气态烷烃和一种气态烯烃组成的混合物共10g,混合气体的密度是相同状况下H2密度的12.5倍.该混合气体通过装有溴水的试剂瓶时,试剂瓶的质量增加了8.4g,该混合气体可能是( )
A.乙烷和乙烯 B.乙烷和乙烯 C.甲烷和乙烯 D.甲烷和丙烯
【答案】C
【解析】
试题分析:混合气体的密度是相同状况下H2密度的12.5倍,则有机物的平均摩尔质量25g/mol,故混合气体中一定有甲烷,混合气体的总的物质的量为![]() =0.4mol.该混合气通过Br2水时,Br2水增重8.4g为烯烃的质量,所以甲烷的质量为1.6g,物质的量为0.1mol,故烯烃的物质的量为0.3mol,结合烯烃的质量和物质的量来确定烯烃的摩尔质量,再根据烯烃组成通式确定烯烃.
=0.4mol.该混合气通过Br2水时,Br2水增重8.4g为烯烃的质量,所以甲烷的质量为1.6g,物质的量为0.1mol,故烯烃的物质的量为0.3mol,结合烯烃的质量和物质的量来确定烯烃的摩尔质量,再根据烯烃组成通式确定烯烃.
解:混合气体的密度是相同状况下H2密度的12.5倍,则有机物的平均摩尔质量25g/mol,烯烃中乙烯的相对分子质量最小为28,故混合气体中一定有甲烷,
混合气体的总的物质的量为![]() =0.4mol.该混合气通过Br2水时,Br2水增重8.4g为烯烃的质量,所以甲烷的质量为1.6g,物质的量为甲烷的物质的量为
=0.4mol.该混合气通过Br2水时,Br2水增重8.4g为烯烃的质量,所以甲烷的质量为1.6g,物质的量为甲烷的物质的量为![]() =0.1mol,故烯烃的物质的量为0.4mol﹣0.1mol=0.3mol,所以M(烯烃)=
=0.1mol,故烯烃的物质的量为0.4mol﹣0.1mol=0.3mol,所以M(烯烃)=![]() =28g/mol,令烯烃的组成为CnH2n,则14n=28,所以n=2,故为乙烯,
=28g/mol,令烯烃的组成为CnH2n,则14n=28,所以n=2,故为乙烯,
所以混合物为甲烷、乙烯,
故选:C.


科目:高中化学 来源: 题型:
【题目】某学习小组进行了如图所示的实验,设第一步HNO3的还原产物只有NO.相关分析不正确的是( )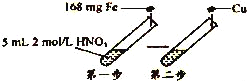
A.第一步反应后溶液中c(NO3﹣)=1.5mol/L(忽略体积变化)
B.第一步反应后溶液中c(Fe2+):c(Fe3+)=1:1
C.第一步可生成标准状况下的气体44.8 mL
D.第二步可溶解铜48mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.汽油与水不相溶,可以用裂化汽油萃取溴水中的溴
B.石油含有烷烃、环烷烃、芳香烃,煤含有苯、甲苯、二甲苯等有机物
C.煤的气化、液化是使煤变成清洁能源,减小环境污染的有效途径
D.沸点范围:汽油>煤油>柴油>重油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的是( )
A. 定容时观察液面俯视
B. 未冷却直接转移溶液
C. 有少量NaOH溶液残留在烧杯中
D. 容量瓶中原来有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)( )
A.乙炔 B.丙炔 C.丁炔 D.丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构,A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性.回答下列问题:
(1)五种元素中,原子半径最大的是 ,非金属性最强的是 (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是____________(用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的电子式为____________;
(4)E的最高价氧化物的水化物的化学式为____________;
(5)单质C在空气中燃烧的产物存在的化学键类型为 ;其反应化学方程式为 ;
(6)单质E与水反应的离子方程式为____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少 8%,氮氧化物(NOx)排放量减少 10%。目前,消除大气污染有多种方法。
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g)△H =-574 kJ/mol
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g)△H =-1160 kJ/mol
③H2O(g) = H2O(l) △H =-44.0 kJ/mol
写出 CH4(g)与 NO2(g)反应生成 N2(g)、CO2(g)和 H2O(l)的热化学方程式:__________。
(2)利用 Fe2+、Fe3+的催化作用,常温下可将 SO2 转化为 SO42-,从而实现对 SO2 的治理。已知含 SO2 的废气通入含 Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为 4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O,则另一反应的 离子方程式为__________。
(3)用活性炭还原法处理氮氧化物。有关反应为 C(s) + 2NO(g) ![]() N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度(mol/L) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
①10~20 min 以υ(N2)表示的反应速率为__________。
②该反应的平衡常数表达式 K=________。根据表中数据,计算 T1 ℃时该反应的平衡常数为__________(保留两位小数)。
③一定温度下,随着 NO 的起始浓度增大,则 NO 的平衡转化率__________ (
④下列各项能作为判断该反应达到平衡的是__________ (填序号)。
A.混合气体的密度保持不变
B.υ正(NO) = 2υ逆(CO2)
C.容器内压强保持不变
D.容器内 N2 的体积分数保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 表示阿伏加德罗常数的值,下列叙述正确的是
A.在反应 KClO3 + 6HCl = KCl + 3Cl2↑+ 3H2O 中,Cl2 既是氧化产物又是还原产物,当得到标准状况下的 67.2 L Cl2 时,反应中转移的电子数为 5NA
B.标准状况下,22.4 L 甲苯中含有的 C—H 键数目为 8NA
C.50 g 46%的乙醇水溶液中,含氢原子总数目为 3NA
D.t℃时,MgCO3 的 Ksp = 4×10-6,则该温度下饱和 MgCO3 溶液中含有的 Mg2+数目为 2×10-3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 钠、钾着火时,不能用泡沫灭火器灭火
B. 氧化铝是冶炼金属铝的原料,也是较好的耐火材料
C. 石英是制造光导纤维的原料,也是常用的半导体材料
D. 在汽车尾气系统中安装催化转化器,可降低尾气中CO、NOx等的排放量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com