
| A. | 常温下,0.1 mol•L-1 CH3COOH溶液的pH=3 | |
| B. | CH3COOH溶液能和NaOH溶液反应 | |
| C. | 往CH3COOH溶液中加入几滴石蕊试液,溶液变红色 | |
| D. | 0.1 mol•L-1CH3COOH溶液做导电性实验,灯光较暗 |
分析 强弱电解质的根本区别是电离程度,部分电离的电解质是弱电解质,只要说明醋酸部分电离就能证明醋酸是弱电解质,据此分析解答.
解答 解:A.常温下,0.1 mol•L-1 CH3COOH溶液的pH=3,氢离子浓度小于醋酸浓度,说明醋酸部分电离,则醋酸为弱电解质,故A正确;
B.醋酸和氢氧化钠反应生成盐和水,说明醋酸是酸,但不能说明醋酸部分电离,所以不能证明醋酸是弱电解质,故B错误;
C.往CH3COOH溶液中加入几滴石蕊试液,溶液变红色,说明醋酸是酸,但不能说明醋酸部分电离,所以不能证明醋酸是弱电解质,故C错误;
D.0.1 mol•L-1CH3COOH溶液做导电性实验,灯光较暗,说明该醋酸中离子浓度降低,但不能说明醋酸部分电离,所以不能证明醋酸是弱电解质,故D错误;
故选A.
点评 本题考查强弱电解质判断,为高频考点,明确强弱电解质根本区别是解本题关键,易错选项是D,电解质溶液导电性强弱与离子浓度有关,与电解质强弱无关,题目难度不大.


科目:高中化学 来源: 题型:选择题
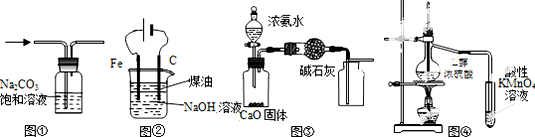
| A. | 图①除去CO2中的HCl | |
| B. | 图②装置制备Fe(OH)2并能较长时间观察其颜色 | |
| C. | 图③所示装置制取并收集干燥纯净的NH3 | |
| D. | 图④证明CH3CH2OH发生消去反应生成了乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀盐酸反应的离子方程式:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Na与水反应的离子方程式:Na+H20═Na++OH-+H2↑ | |
| C. | FeCl3中加入统分的离子方程式:2Fe3++Cu═2Fe2++Cu2+ | |
| D. | 醋酸的电离方程式:CH3COOH═CH3COO-+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
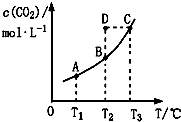
| A. | 该反应的△H<0 | |
| B. | 在T2时,D点的反应速率:ν(正)<(逆) | |
| C. | A、C两点相比,混合气体的平均相对分子质量:M(A)<M(C) | |
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1>K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 外界条件相同时,放热反应的速率一定大于吸热反应的速率 | |
| B. | 化学反应中的能量变化可表现为热量的变化 | |
| C. | 反应物的总能量高于生成物的总能量时,发生放热反应 | |
| D. | CaO+H2O═Ca(OH)2反应过程中,旧键断裂吸收的能量小于新键形成释放的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有0.1mol•L-1CO32-的溶液:Na+、Al3+、NO3-、S2- | |
| B. | 无色溶液:K+、H+、SCN-、SO42- | |
| C. | $\frac{Kw}{c{(H}^{+})}$=0.1mol/L的溶液:Na+、K+、HCO3-、NO3- | |
| D. | 在由水电离出的c(H)=1.0×10-13mol•L-1的溶液中:Na+、Fe3+、Cl-、CH3COO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com