
按要求完成下列问题:
(1)0.5 mol H2O的质量为 g,共有____________个分子。
(2) 0.01mol某物质的质量为1.08g,则此物质的摩尔质量为__________________。
(3)配制50 mL 0.2 mol·L—1 CuSO4溶液,需要CuSO4_____________g。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届山东省潍坊市高一上学期期末统考化学试卷(解析版) 题型:填空题
将10.7g 氯化铵固体与足量熟石灰混合加热,使之充分反应。
(1)写出反应的化学方程式: 。
(2)生成的氨气在标准状况下的体积是 L。
(3)若将这些氨气溶于水配成500mL氨水,该氨水的物质的量浓度是 mol·L-1。
(4)在400℃左右且有催化剂存在的情况下,用氨可以把一氧化氮还原成氮气,方程式为:4NH3+6NO=5N2+6H2O,此反应中氧化产物与还原产物的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省济宁市高一12月质检化学试卷(解析版) 题型:计算题
有铁和铝的混合物共5.5g,完全溶解于200mL 36.5%的浓盐酸(密度为1.2 g/mL)中,在标准状况下共收集到4.48L H2,求:
(1)浓盐酸的物质的量浓度为 。
(2)铁的质量为 ,铝的质量为 。
(3)将反应后剩余的溶液,用水稀释至500mL,求稀释后溶液中盐酸的物质的量浓度(HCl挥发忽略不计) 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省济宁市高一12月质检化学试卷(解析版) 题型:选择题
下列各组离子中,能在溶液中大量共存的是
A.OH- Na+ HCO3- Cl- B.Ba2+ Na+ Cl- SO42-
C.K+ Al3+ SO42- OH- D.Ag+ Al3+ NO3- H+
查看答案和解析>>
科目:高中化学 来源:2016届山东省泰安市高一上学期期末考试化学试卷(解析版) 题型:填空题
实验室用图I所示的装置制取干燥的氨气。
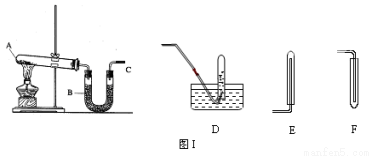
(1)A处反应的化学方程式为 。
(2)为收集到干燥的氨气,导管C应接 (填序号)。
(3)装置B中盛装的试剂的名称是 。
(4)在水槽中加入水(含酚酞),将充满氨气的试管倒置于放入水槽中(如图Ⅱ所示),将拇指稍移开试管口,可观察到的现象为_______________ 。
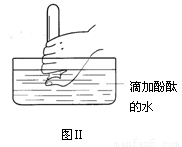
(5)在D、E、F三种气体收集方法中,能用于收集NO的是________(填写序号)。
查看答案和解析>>
科目:高中化学 来源:2016届山东省泰安市高一上学期期末考试化学试卷(解析版) 题型:选择题
海藻中含有丰富的碘元素。下图是实验室从海藻里提取碘的流程的一部分。下列判断正确的是
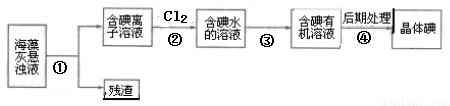
A.步骤④的操作是过滤
B.可用淀粉溶液检验步骤②的反应是否进行完全
C.步骤①、③的操作分别是过滤、萃取
D.步骤③中加入的有机溶剂可能是酒精或CCl4
查看答案和解析>>
科目:高中化学 来源:2016届山东省泰安市高一上学期期末考试化学试卷(解析版) 题型:选择题
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种。若该气体为无色气体,且通过品红溶液后,品红溶液褪色,剩余气体与空气接触时,很快变为红棕色。下列判断正确的是
A.肯定只有NO B.肯定有SO2和NO2
C.可能有Cl2和O2 D.肯定没有Cl2、O2和NO2
查看答案和解析>>
科目:高中化学 来源:2016届山东省高一上学期期中考试化学试卷(解析版) 题型:选择题
已知常温下在溶液中可发生如下两个离子反应:
Ge4++Fe2+=Fe3++Ge3+ ①;Sn2++2Fe3+=2Fe2++Sn4+ ②
由此可以确定Fe2+、Ge3+、Sn2+三种离子的还原性由强到弱的顺序是
A.Sn2+、Fe2+、Ge3+ B.Sn2+、Ge3+、Fe2+
C.Ge3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ge3+
查看答案和解析>>
科目:高中化学 来源:2016届天津市五区县高一上学期期末考试化学试卷(解析版) 题型:填空题
食盐、碳酸钠和碳酸氢钠是生活中常见的钠盐。请回答下列问题。
(1)碳酸氢钠的水溶液显__________性。(填“酸”、“碱”或“中”)。除去碳酸钠固体中混有的少量碳酸氢钠,反应的化学方程式为_________________。
(2)等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成的CO2量,前者________后者(填“>”、“<”或“=”)。
(3)粗盐含有少量杂质(主要为CaCl2、MgCl2、Na2SO4等)。用粗盐制取“化学纯”级的NaCl,步骤为溶解、加过量a、加过量NaOH、加过量b、过滤、加适量盐酸,蒸发结晶得到“化学纯”级的NaCl固体。试剂a、b分别是________(填序号)
A.Na2CO3 BaCl2 B.BaCl2 Na2CO3 C.BaCl2 Na2SO4
(4)工业上用电解饱和食盐水的方法生产氯气和烧碱。
①某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理_________________________________(用离子方程式表示)。
②工业上可用氨检验输送氯气的管道是否漏气。反应方程式如下:
 该反应中,____________元素被还原;该反应中氧化剂和还原剂物质的量之比为__________。
该反应中,____________元素被还原;该反应中氧化剂和还原剂物质的量之比为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com