
| 10 |
| 4 |
| 10 |
| 4 |
| 42 |
| 14 |


科目:高中化学 来源: 题型:
 气态有机物 A在标准状况下密度为1.25g/L,A在一定条件下可以合成聚合物B,B可作食品包装袋.
气态有机物 A在标准状况下密度为1.25g/L,A在一定条件下可以合成聚合物B,B可作食品包装袋.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)铝热反应原理
(1)铝热反应原理| 实验步骤 | 现象 | 结论 |
| ①取少量黑色固体于试管中加稀盐酸 | 固体全部溶解,有气泡产生 | 假设Ⅰ成立,假设Ⅱ不成立 |
| ②滴入几滴0.01mo1/L KSCN溶液 | 深液不变色 |
| 编号 | 实验步骤 |
| 1 | ①滴加饱和FeC13溶液4滴,充分振荡 |
| ②滴加几滴NaOH溶液 | |
| 2 | ①滴加4滴1mol?L-1 KSCN溶液 |
| ②滴加几滴NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
1 1 |
2 1 |
3 1 |
1 1 |
2 1 |
3 1 |
 与
与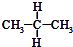
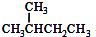 与
与
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合气体颜色保持不变 |
| B、体系压强保持不变 |
| C、SO3和NO的体积比保持不变 |
| D、每消耗1 mol SO3的同时生成1 mol NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气的摩尔质量是71克 |
| B、HCl的摩尔质量为36.5 g/mol |
| C、1摩氢气的质量为2 g/mol |
| D、O2的摩尔质量为16g/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com