
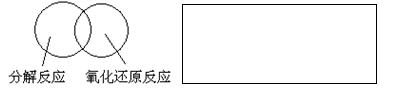
 (3)有一瓶澄清的溶液,其中可能含有H+、NH+4、Mg2+、Ba2+、Al3+、I-、NO-3、CO2-3、SO2-4、AlO-2,取该溶液进行以下实验:
(3)有一瓶澄清的溶液,其中可能含有H+、NH+4、Mg2+、Ba2+、Al3+、I-、NO-3、CO2-3、SO2-4、AlO-2,取该溶液进行以下实验: 溶液,有白色沉淀生成,证明______存在,又排除________存在。
溶液,有白色沉淀生成,证明______存在,又排除________存在。 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO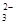 SO SO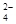 |
 酸。
酸。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 +3H2O。下列叙述正确的是
+3H2O。下列叙述正确的是| A.上式中缺项所填物质在反应中作氧化剂 | B.R的原子半径在同周期元素原子中最小 |
| C.R一定是周期表中的第VA族元素 | D.RO3-中的R元素在所有的反应中只能被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


 (HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,反应的离子方程式_________________________在上述溶液中继续滴入NaHSO4溶液,此时离子方程式为_______________________。
(HCO3)2溶液中滴入NaHSO4溶液,至沉淀完全,反应的离子方程式_________________________在上述溶液中继续滴入NaHSO4溶液,此时离子方程式为_______________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 )
)| A. K2CO3、BaCl2 | B.NaOH、CuSO4 |
| C. AgNO3、NaCl | D. Na2CO3、CaCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 含有的物质是 (以上物质均写化学式),写出第①步中反应的化学方程式:
含有的物质是 (以上物质均写化学式),写出第①步中反应的化学方程式:  ,
,查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲溶液中c(CH3COO-)一定大于乙溶液中c(CH3COO-) |
| B.甲、乙等体积混合后pH大于2 |
| C.乙溶液离子浓度大小关系为:c(Cl-)>c(CH3COO-)> c(H+)>c(OH-) |
| D.加入相同浓度的NaOH溶液至中性,甲乙两溶液消耗NaOH溶液的体积相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com