
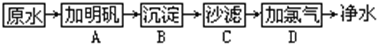
分析 ⅰ、(1)过滤分离可溶物和不溶物;
(2)氯气与水反应生成的次氯酸有强氧化性;
ⅱ、①碳酸钙不溶于水,食盐溶于水;
②溴不易溶于水,易溶于有机溶剂;
③二者互溶,但沸点不同;
④水易挥发;
⑤水易挥发;
⑥油水不溶.
解答 解:ⅰ、(1)在净化水时,通过过滤可以除去大量颗粒悬浮物杂质,故答案为:C;
(2)氯气与水反应生成的次氯酸有强氧化性,能起到消毒杀菌的作用,故答案为:D;
ⅱ、①碳酸钙不溶于水,食盐溶于水,则选择过滤法分离,故答案为:溶解、过滤;②溴不易溶于水,易溶于有机溶剂,则选择萃取法从溴水中分离出溴,故答案为:萃取、分液;
③乙醇和水互溶,但沸点不同,则选择蒸馏法分离,故答案为:蒸馏;
④水易挥发,氯化钠难挥发,可用蒸发分离,故答案为:蒸发;
⑤水易挥发,蒸馏可得到蒸馏水,故答案为:蒸馏;
⑥油水不溶,可用分液分离,故答案为:分液.
点评 本题考查混合物的分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
 2Fe3O4(S)+C.
2Fe3O4(S)+C.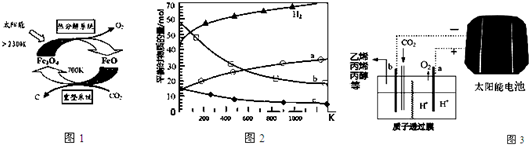
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.25 mol H2SO4 | B. | 1 mol H2O | C. | 40 g CaO | D. | 80 g Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )| A. | 工业上,B转化为D的反应条件为高温、高压、使用催化剂 | |
| B. | 若A为铁,则足量A与X在室温下即可发生反应 | |
| C. | 若A为碳单质,则将少量C通入足量NaClO溶液中,产物为NaHCO3和HClO | |
| D. | X使蔗糖变黑的现象主要体现了X的强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某反应由两步反应A═B═C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能).下列有关叙述正确的是( )
某反应由两步反应A═B═C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能).下列有关叙述正确的是( )| A. | 两步反应均为放热反应 | |
| B. | 三种化合物的稳定性顺序:B<A<C | |
| C. | 整个反应的△H=E1-E2 | |
| D. | 加入催化剂不改变反应的焓变,但能提高产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 DDT又叫滴滴涕,化学名为双对氯苯基三氯乙烷,化学式(ClC6H4)2CH(CCl3).名称从英文缩写DDT而来,为白色晶体,不溶于水,溶于煤油,可制成乳剂,是有效的杀虫剂.DDT进入食物链,是导致一些食肉和食鱼的鸟接近灭绝的主要原因.因此从70年代后滴滴涕逐渐被世界各国明令禁止生产使用.其结构为:下列有关说法正确的是( )
DDT又叫滴滴涕,化学名为双对氯苯基三氯乙烷,化学式(ClC6H4)2CH(CCl3).名称从英文缩写DDT而来,为白色晶体,不溶于水,溶于煤油,可制成乳剂,是有效的杀虫剂.DDT进入食物链,是导致一些食肉和食鱼的鸟接近灭绝的主要原因.因此从70年代后滴滴涕逐渐被世界各国明令禁止生产使用.其结构为:下列有关说法正确的是( )| A. | DDT属于卤代烃类 | |
| B. | DDT完全燃烧后只产生CO2和H2O两种物质 | |
| C. | DDT分子中有一个手性碳 | |
| D. | 氢核磁共振谱图中有5种位置峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
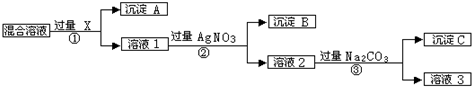
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是放热反应都是自发反应,凡是吸热反应都是不自发的反应 | |
| B. | 凡是熵增大的过程都是自发的,凡是熵减小的过程都是不自发的 | |
| C. | 一个自发倾向很大的反应在常温下就很容易进行 | |
| D. | 一个熵值减小的吸热反应在任何温度都是不自发的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com