
| | A | B | C | D |
| 电极材料 | Cu、Zn | Cu、Ag | Cu、C | Fe、Zn |
| 电解液 | FeCl3 | Fe2(SO4)3 | Fe(NO3)2 | CuSO4 |
科目:高中化学 来源:不详 题型:填空题
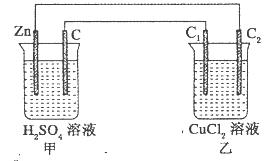
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
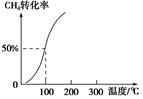
 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。| A.c(H2)减少 |
| B.正反应速率加快,逆反应速率减慢 |
| C.CH3OH 的物质的量增加 |
| D.重新平衡c(H2)/c(CH3OH)减小 |
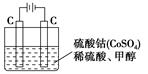
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.I2+2Rb++2e-=2RbI |
| B.I2+2Ag++2e-=2AgI |
| C.Ag-e-=Ag+ |
| D.4AlI3+3O2=2Al2O3+6I2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
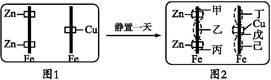
| A.甲区呈现蓝色 | B.乙区呈现红色 |
| C.戊区产生Cu2+离子 | D.丁区产生Fe3+离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
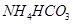 溶液呈碱性,30℃以上溶液中
溶液呈碱性,30℃以上溶液中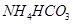 大量分解。
大量分解。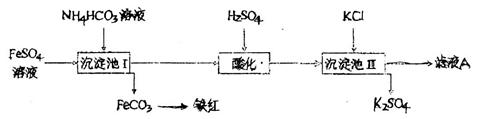
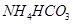 溶液中的物料守恒___________________________________
溶液中的物料守恒___________________________________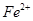 沉淀是否完全的方法是__________________________________。
沉淀是否完全的方法是__________________________________。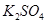 晶体分离出来用到过滤操作,过滤时用到的主要玻璃仪器是__________________________。
晶体分离出来用到过滤操作,过滤时用到的主要玻璃仪器是__________________________。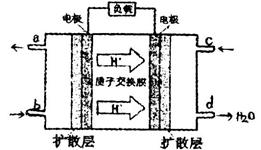
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
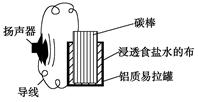
| A.碳棒上发生的主要反应为:2H++2e-=H2↑ |
| B.铝质易拉罐将逐渐得到保护 |
| C.电池总反应为:4Al+3O2+6H2O==4Al(OH)3 |
| D.电子方向为:铝质易拉罐→导线→扬声器→导线→碳棒→浸透食盐水的布 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
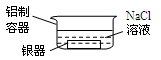
| A.铝质容器为正极,银器为负极 |
| B.反应前后银器质量不变 |
| C.Ag2S被还原生成单质银 |
| D.总反应为2Al+3Ag2S → 6Ag+ Al2S3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.原电池是将化学能转化为电能的装置 |
| C.在原电池中,电子流出的一极是负极,该电极被还原 |
| D.原电池放电时,电流的方向是从负极到正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com