
| 20g-3.2g |
| 56g/mol |
| 8.96L |
| 22.4L/mol |
|
| 1mol |
| 0.5L |
| 0.3mol��2 |
| 4 |
| 8 |
| 3 |
| 6 |
| 3 |
| 2 |
| 3 |
| 0.36mol |
| 0.1L |
| 0.4mol |
| 0.1L |
| 8 |
| 3 |
| 8n |
| 3 |
| 6 |
| 3 |
| 2 |
| 3 |
| 4n |
| 3 |
| 8n |
| 3 |
| 4n |
| 3 |
| 4n |
| 3 |
(0.2+
| ||
| 0.1L |
| 40n |
| 3 |
| 40n |
| 3 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
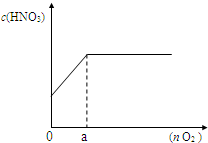 ��2011?������һģ����500mL ijŨ�ȵ�������Һ�м���20g���ۣ���ַ�Ӧ����ӦҺ���ˡ�ϴ�ӡ�����Ƶù�������Ϊ3.2g��������NO2��NO���徭�ⶨΪ8.96L����״������
��2011?������һģ����500mL ijŨ�ȵ�������Һ�м���20g���ۣ���ַ�Ӧ����ӦҺ���ˡ�ϴ�ӡ�����Ƶù�������Ϊ3.2g��������NO2��NO���徭�ⶨΪ8.96L����״������| 40n |
| 3 |
| 40n |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij����С����MnO2��Ũ�����Ʊ�Cl2ʱ�����ø����չ�����SO2��NaOH��Һ����β���������մ�����
��1�������SO2�����NaOH��Һ��Ӧ�Ļ�ѧ����ʽ�� ________________��
��2����ӦCl2+Na2SO3+2 NaOH===2NaCl+Na2SO4+H2O�еĻ�ԭ��Ϊ_________��
��3�������MnO2��Ũ�����Ʊ�Cl2�����ӷ���ʽ�� _______ _________��
��4�����14.2g������������������Ӧ��Ȼ�����ɵ�������500mLijŨ�ȵ�NaOH��Һǡ�÷�Ӧ�����NaOH��Ũ��Ϊ ����д��������̣�
��5������β��һ��ʱ�������Һ��ǿ���ԣ��п϶�����Cl![]() ��OH
��OH![]() ��SO
��SO![]() �������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
�������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
������������� ��
����1��ֻ����SO32-������2���Ȳ�����SO32-Ҳ������ClO![]() ������3��SO32-��ClO
������3��SO32-��ClO![]() �����ڡ�
�����ڡ�
���ʵ�鷽��������ʵ�顣���ڴ����д����ʵ�鲽����Ӧ��Ԥ������ͽ��ۡ���ѡʵ���Լ���3moL![]() L-1H2SO4��1moL
L-1H2SO4��1moL![]() L-1NaOH��0.01mol
L-1NaOH��0.01mol![]() L-1KMnO4������-KI��Һ����ɫʯ����Һ��
L-1KMnO4������-KI��Һ����ɫʯ����Һ��
| ʵ�鲽�� | Ԥ������ͽ��� |
|
| |
| ����2����A�Թ��еμ���ɫʯ����Һ | |
| ����3����B�Թ��еμ�0.01mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij����С����MnO2��Ũ�����Ʊ�Cl2ʱ�����ø����չ�����SO2��NaOH��Һ����β���������մ�����
��1�������SO2�����NaOH��Һ��Ӧ�Ļ�ѧ����ʽ�� ________________��
��2����ӦCl2+Na2SO3+2NaOH===2NaCl+Na2SO4+H2O�еĻ�ԭ��Ϊ_________��
��3�������MnO2��Ũ�����Ʊ�Cl2�����ӷ���ʽ�� _______ _________��
��4�����14.2g������������������Ӧ��Ȼ�����ɵ�������500mLijŨ�ȵ�NaOH��Һǡ�÷�Ӧ�����NaOH��Ũ��Ϊ ����д��������̣�
��5������β��һ��ʱ�������Һ��ǿ���ԣ��п϶�����Cl![]() ��OH
��OH![]() ��SO
��SO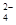 �������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
�������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
������������� ��
����1��ֻ����SO32-������2���Ȳ�����SO32-Ҳ������ClO ������3��SO32-��ClO
������3��SO32-��ClO![]() �����ڡ�
�����ڡ�
���ʵ�鷽��������ʵ�顣���ڴ����д����ʵ�鲽����Ӧ��Ԥ������ͽ��ۡ���ѡʵ���Լ���3moL L-1H2SO4��1moL
L-1H2SO4��1moL L-1NaOH��0.01mol
L-1NaOH��0.01mol![]() L-1KMnO4������-KI��Һ����ɫʯ����Һ��
L-1KMnO4������-KI��Һ����ɫʯ����Һ��
| ʵ�鲽�� | Ԥ������ͽ��� |
|
|
|
| ����2����A�Թ��еμ���ɫʯ����Һ |
|
| ����3����B�Թ��еμ�0.01mol |
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011���Ϻ��г����ظ߿���ѧһģ�Ծ��������棩 ���ͣ������
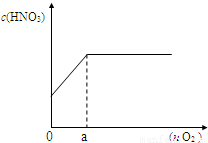
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com