
| A. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| B. | 戊烷(C5H12)有两种同分异构体 | |
| C. | 糖类、油脂和蛋白质均可发生水解反应 | |
| D. | 油脂皂化反应得到高级脂肪酸盐与甘油 |
分析 A.聚氯乙烯、苯中都不含碳碳双键;
B.戊烷的同分异构体有正戊烷、异戊烷和新戊烷三种同分异构体;
C.单糖不能发生水解反应;
D.油脂在碱性条件下水解生成甘油和高级脂肪酸盐,在酸性条件下生成高级脂肪酸和甘油.
解答 解:A.聚氯乙烯、苯中都不含碳碳双键,苯中含有大π键,只有乙烯中含有碳碳双键,故A错误;
B.戊烷的同分异构体有正戊烷、异戊烷和新戊烷三种同分异构体,所以其同分异构体有3种,故B错误;
C.单糖不能发生水解反应,二糖、多糖、蛋白质和油脂都能发生水解反应,故C错误;
D.油脂在碱性条件下水解生成甘油和高级脂肪酸盐,在酸性条件下生成高级脂肪酸和甘油,油脂在酸性或碱性条件下都生成甘油,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确物质结构特点、物质性质是解本题关键,注意聚乙烯中不含碳碳双键但聚乙炔中含有碳碳双键,为易错点.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 石油分馏、煤的气化、煤的干馏、海水制盐等都属于化学变化过程 | |
| B. | 在牙膏中添加Na2PO3F、NaF能防治龋齿,当提供的F-浓度相等时,它们防治龋齿的作用是相同的 | |
| C. | NO2、SO2、CO2、PM2.5都是空气质量日报必须报道的大气污染物 | |
| D. | 家用天然气含有特殊气味的主要原因是开采的天然气未经处理就直接转为民用燃气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
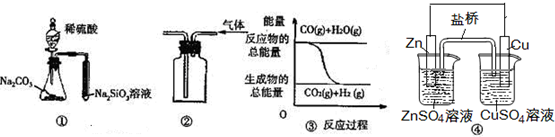
| A. | 图 ④中的装置可形成持续稳定的电流.将锌片浸入CuSO4溶液中发生的化学反应与图 ④中的原电池装置反应不相同 | |
| B. | 用图 ②所示实验装置排空气法收集H2气体 | |
| C. | 图 ③表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为放热反应 | |
| D. | 用图 ①所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
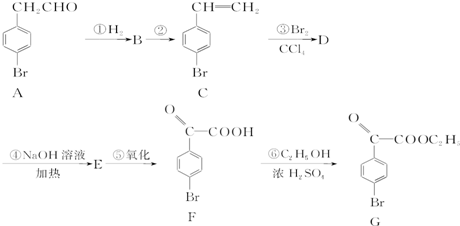
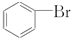 在NaOH溶液中很难水解.
在NaOH溶液中很难水解.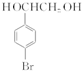 .
.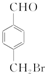 、
、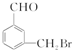 、
、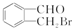 .
.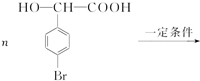
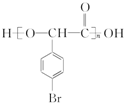 +(n-1)H2O.
+(n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
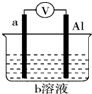 如图是某同学设计的一个简易的原电池装置,回答下列问题.
如图是某同学设计的一个简易的原电池装置,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 3 | ① | ③ | ④ | ⑨ | ||||
| 4 | ② |
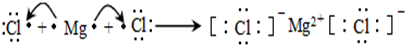 .
.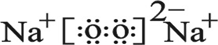 ,该物质所含化学键类型离子键和共价键,0.1mol X与水反应转移电子数为:0.1NA.
,该物质所含化学键类型离子键和共价键,0.1mol X与水反应转移电子数为:0.1NA.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
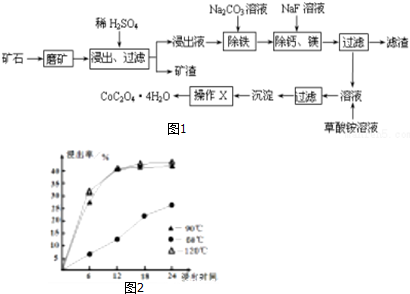
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com