
【题目】已知FeS与某浓度的HNO3反应时生成Fe(NO3)3、H2SO4和某一单一的还原产物,若FeS和参与反应的HNO3的物质的量之比为1︰6,则该反应的还原产物是
A. NO B. NO2 C. N2O D. NH4NO3
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学,是研究物质的性质的重要途径。某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
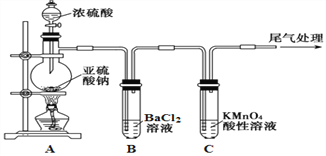
已知:Na2SO3+H2SO4(浓)![]() Na2SO4+SO2↑+H2O,请回答下列问题:
Na2SO4+SO2↑+H2O,请回答下列问题:
(1) 装置A中盛放浓硫酸的仪器名称是__________________。
(2) 实验过程中,C中的现象是____________,说明SO2具有_________性。
(3) 实验过程中,观察到装置B中出现了明显的白色沉淀。为探究该白色沉淀的成分,该小组同学进行了如下实验:
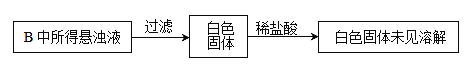
根据实验事实判断该白色沉淀的成分是_______________(填化学式),产生该白色沉淀的原因可能是_____________(填字母编号)。
a.BaSO3既不溶于水也不溶于酸
b.BaCl2溶液中可能溶解有氧气
c.BaCl2溶液中可能混有NaOH
d.由A制得的SO2气体中可能混有氧气
(4)如果将装置A中的浓H2SO4换作浓HNO3,对此实验是否有影响并说明理由_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4 ℃,熔点9.79 ℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
填写下列空白:
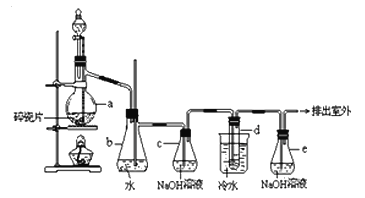
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式: 。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象: 。
(3)容器c中NaOH溶液的作用是: 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物说法正确的是
A. 乙醇、乙烷和乙酸都可以与钠反应生成氢气
B. 75%(体积分数)的乙醇溶液常用于医疗消毒
C. 苯和乙烯都可使溴的四氯化碳溶液褪色
D. 石油分馏可获得乙酸、苯及其衍生物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量存在的离子组是
A.Mg2+、 NH4+、Cl- B.Mg2+、Ba2+、Br-
C.Na+、C1-、I- D.Al3+、HCO3-、C1-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2—叔丁基对苯二酚是一种重要的食品抗氧剂,现以对苯二酚、叔丁醇为原料,一定条件下经Freidel-Crafts 烷基化反应合成。原理如下:
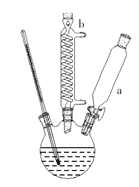
步骤Ⅰ:连接如右图所示装置。
步骤Ⅱ:向三颈烧瓶中加入4.0g 对苯二酚,15mL 浓磷酸,15mL甲苯,启动搅拌器,油浴加热混合液至90℃。从仪器a缓慢滴加 3.5mL叔丁醇,使反应温度维持在 90℃~95℃,并继续搅拌 15min 至固体完全溶解。
步骤Ⅲ:停止搅拌,撤去热浴,趁热转移反应液至分液漏斗中,将分液后的有机层转移到三颈烧瓶中,加入 45mL 水进行水蒸气蒸馏,至无油状物蒸出为止。
步骤Ⅳ:把残留的混合物趁热抽滤,滤液静置后有白色晶体析出,
最后用冷水浴充分冷却,抽滤,晶体用少量冷水洗涤两次,压紧、抽干。
⑴图中仪器a的名称为_____________;仪器b的作用是_____________。
⑵步骤Ⅱ中所加入物质中,有一种物质是催化剂,其化学式为_____________。
⑶已知:叔丁醇熔点是 25℃~26℃,常温下是固体。实验时加入叔丁醇的方法是
_____________。
⑷制备过程应严格控制反应温度90℃~95℃,其原因是_____________。
⑸2—叔丁基对苯二酚粗产品久置会变红,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
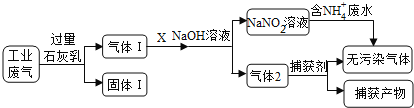
(1)固体I中主要成分为__________,捕获剂所捕获的气体主要是_________。
(2)处理含NH4+废水时,发生反应的离子方程式为___________。
(3)若X为适量空气,严格控制空气用量的原因是____________。
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
c(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_________________。
增加压强,NO的转化率__________(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐__________(填“增大”、“不变”或“减小”)。
③如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B![]() 2C。若维持温度和压强不变,当达到平衡时容器的体积为VL,其中C气体的体积占10%。下列推断正确的是 ( )
2C。若维持温度和压强不变,当达到平衡时容器的体积为VL,其中C气体的体积占10%。下列推断正确的是 ( )
①原混合气体的体积为1.2V L
②原混合气体的体积为1.1V L
③反应达到平衡时气体A消耗掉0.05VL
④反应达平衡时气体B消耗掉0.05V L
A.①③ B.②③ C.①④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表部分短周期元素信息,判断以下叙述正确的是( )

A. 氢化物的沸点为H2T<H2R B. 单质与稀盐酸反应的剧烈程度L<Q
C. M与T形成的化合物具有两性 D. L2+与R2﹣的核外电子数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com