
| A. | 0.lmol Fe在0.lmolCl2中充分燃烧,转移的电子数为0.3NA | |
| B. | 25℃时,pH=13的1.0 LBa(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 含NA个氧原子的O2与含NA个氧原子的O3的质量比为2:3 | |
| D. | lmol CnH2n+2分子中含共价键数目为(3n+1)NA |
分析 A.铁与氯气反应生成氯化铁,氯气不足依据氯气的量计算电子转移数;
B.依据体积和氢氧根离子浓度计算物质的量;
C.臭氧与氧气都是由氧原子构成,依据n=$\frac{m}{M}$计算解答;
D.1个CnH2n+2分子中含有n-1个C-C键,含有2n+2个H-C键.
解答 解:A.0.lmol Fe在0.lmolCl2中充分燃烧,完全反应生成0.2mol氯离子,转移的电子数为0.2NA,故A错误;
B.溶液的pH=13,故C(H+)=10-13mol/L,可知C(OH-)=0.1mol/L,溶液体积为1.0L,故含有的氢氧根的物质的量为0.1mol,个数为0.1NA,故B错误;
C.臭氧与氧气都是由氧原子构成,含NA个氧原子的O2与含NA个氧原子的O3的质量比为1;1,故C错误;
D.1个CnH2n+2分子中含有n-1个C-C键,含有2n+2个H-C键,所以lmol CnH2n+2分子中含共价键数目为(3n+1)NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,注意有机物结构组成,题目难度不大.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 水、四氯化碳、苯 | B. | AgNO3、NaOH、KI | C. | NaCl、NaBr、NaI | D. | 汽油、酒精、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘酒能消毒是利用碘的还原性 | |
| B. | 葡萄糖注射液不能产生丁达尔效应,不属于胶体 | |
| C. | 14C可用于文物的年代鉴定,14C与12C互为同素异形体 | |
| D. | 某溶液中加盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和石灰水跟稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O | |
| B. | 除去硫酸铁溶液中的亚铁离子:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 将数滴0.lmol/L盐酸溶液缓缓滴入lmol/L50mLNa2CO3溶液中,且不断搅拌:2H++CO32-═H2O+CO2↑ | |
| D. | 向NaHSO4溶液中滴加Ba(OH)2溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠是一种强还原剂,可以将钛、铌等金属从其氯化物溶液中置换出来 | |
| B. | 铜能与氯化铁溶液反应,该反应可以应用于印刷电路板的制作 | |
| C. | 人们发现了118种元素,即共有118种核素 | |
| D. | H2和D2互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | c2 | c3 | c3 |
| 4 | C1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
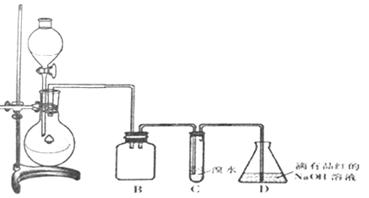
| 实验序号 | 实验操作 | 现象 | 可能的情况 |
| ① | 滴加少量淀粉-KI溶液,振荡 | III | |
| ② | 滴加少量溴水,振荡 | II | |
| ③ | 滴加少量酸性KMnO4溶液,振荡 | 溶液呈紫色 | |
| ④ | 加入几小块CaCO3固体 | 有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
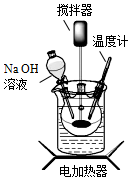 超细Fe3O4粉体可制成磁流体,一种制备超细Fe3O4粉体的实验步骤如下:
超细Fe3O4粉体可制成磁流体,一种制备超细Fe3O4粉体的实验步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com