
【题目】电解质溶液的电导率越大,导电能力越强。用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是

A. 曲线①代表滴定CH3COOH溶液的曲线
B. A、C两点对应溶液均呈中性
C. B点溶液中:c(Na+) > c(OH-) > c(CH3COO-)
D. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.050mol/L
【答案】B
【解析】溶液导电能力与离子浓度成正比,CH3COOH是弱电解质,溶液中离子浓度较小,加入KOH后,溶液中离子浓度增大,溶液导电性增强;HCl是强电解质,随着KOH溶液加入,溶液体积增大,导致溶液中离子浓度减小,溶液导电能力减弱,当完全反应式离子浓度最小,继续加入KOH溶液,离子浓度增大,溶液导电能力增强,根据图知,曲线②代表0.1 mol/L NaOH溶液滴定HCl溶液的滴定曲线,曲线①代表0.1 mol/LKOH溶液滴定CH3COOH溶液的滴定曲线,A.由分析可知,曲线①代表滴定CH3COOH溶液的曲线,选项A正确;B.A点溶质为醋酸钠,醋酸钠水解溶液呈碱性,C点溶质为NaCl,溶液呈中性,选项B不正确;C、B点为等物质的量浓度的醋酸钠和NaOH,c(Na+)最大 ,CH3COO-水解产生OH-,c(OH-) > c(CH3COO-),故c(Na+) > c(OH-) > c(CH3COO-),选项C正确; D.A点溶液中c(Na+)=0.05mol/L,电解质溶液中都存在电荷守恒,根据电荷守恒得c(CH3COO-)+c(OH-)-c(H+)=c(Na+)=0.05mol/L,选项D正确。答案选B。


科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( ) 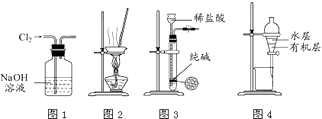
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据硫酸所具有的性质,选择适当的字母按要求填空. A、吸水性B、脱水性C、强氧化性
(1)用玻璃棒蘸浓硫酸滴在纸上,发现变黑,说明浓硫酸具有;
(2)浓硫酸常用作干燥剂,说明浓硫酸具有;
(3)浓硫酸都可以与铜反应,反应中浓硫酸和浓硝酸显示出 .
查看答案和解析>>
科目:高中化学 来源: 题型:
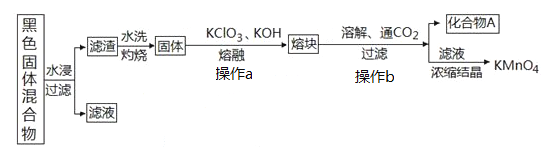
【题目】下图表示从废旧普通锌锰电池内容物中回收制备KMnO4等物质的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。
(1)KMnO4稀溶液是一种常用消毒剂,其消毒机理与下列物质相似的是______________(填序号)
A.双氧水 B.75%酒精 C.苯酚 D.84消毒液(NaClO溶液)
(2)①黑色固体混合物水浸时为提高浸出速率,常采用的措施为_________________(答出两条即可)。
②滤渣水洗灼烧后固体是一种黑色的化合物,操作a中得到熔块的主要成分是K2MnO4和KCl,该过程中发生反应的化学方程式为:_____________________________。
③图中产物A是一种难溶于水的黑色固体,其化学式为:_________________。
(3)测定KMnO4产品的纯度可用标准Na2S2O3溶液进行滴定。
①配制250mL0.1000mol·L-1标准Na2S2O3溶液,需要使用的玻璃仪器有烧杯、胶头滴管、量筒和______、_______;
②取上述制得的KMnO4产品0.7000g,酸化后用0.1000mol·L-1标准Na2S2O3溶液进行滴定,滴定至终点记录实验消耗Na2S2O3溶液的体积,重复步骤②,三次平行实验数据如下表。
实验次数 | 1 | 2 | 3 |
消耗Na2S2O3溶液体积/mL | 19.30 | 20.98 | 21.02 |
(有关离子方程式为:MnO4-+S2O32-+H+—SO42-+Mn2++H2O,未配平)
将0.1000mol·L-1标准Na2S2O3溶液盛装在________(填“酸式”或“碱式”)滴定管中进行滴定。计算该KMnO4产品的纯度_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沼气是一种廉价的能源.农村富有大量的秸杆、杂草[主要成分纤维素化学式为(C6H10O5)n]等废弃物,它们经微生物发酵之后,便可产生沼气,可用来点火做饭.
(1)已知:(C6H10O5)n[纤维素]+nH2O=3nCO2+3nCH4+能量,请设想出这个总反应的实际价值与意义 .
(2)煤的主要成分是碳,写出煤和沼气中的主要成分燃烧的化学方程式 , , 并指出哪一种燃料对环境污染小;
(3)目前,我国农村大约有700万个沼气池,如果每个沼气池每天平均产生2m3沼气(主要成分是CH4)700万个沼气池每天燃烧所放出的热量,相当于1.66×107Kg标准煤的燃烧值,请你再说明使用沼气发生池还有哪些优点?
(4)若建立沼气池发电站,可以实现把能转化成电能.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铝及其化合物说法,不正确的是( )
A.明矾可用作净水剂和消毒剂B.利用铝热反应可冶炼高熔点金属
C.铝可用作包装材料和建筑材料D.氢氧化铝可用作治疗胃酸过多的药物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵[aFe2(SO4)3b(NH4)2SO4cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等.某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如图工艺流程制取硫酸铁铵. 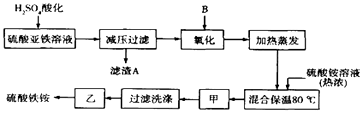
请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是
(2)下列物质中最适合的氧化剂B是 .
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲的名称是:甲 .
(4)上述流程中,氧化之后和加热蒸发之前,需取少量(填试剂的化学式)检验Fe2+是否已全部被氧化;
(5)称取14.00g所得样品,将其溶于水配制成100mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14g沉淀;向另一份溶液中加入0.05mol Ba (NO3)2溶液,恰好完全反应.则该硫酸铁铵的化学式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com