
| A、该溶液中含有SO42- 的物质的量为1mol | B、该溶液中含有溶质Na2SO4的质量为142g | C、将1molNa2SO4固体溶于1L 水配得该溶液 | D、从1L该溶液中取出500mL后,剩余溶液的物质的量浓度为0.5 mol/L |


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:阅读理解

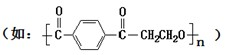 做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是
做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是查看答案和解析>>
科目:高中化学 来源: 题型:
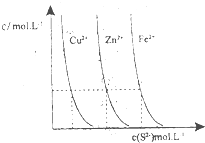 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题:| 弱酸化学式 | CH3COOH | HCN | H2CO |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
| 放电 |
| 通电 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年陕西省三原县北城中学高二上学期期中考试化学试卷(带解析) 题型:单选题
对1L 1mol·L-1的NH4Cl溶液进行如下操作,溶液的pH增大的是( )
| A.加热 | B.加水稀释 |
| C.加入少量的NH4Cl固体 | D.再加1L 1mol·L NH4Cl溶液 |
查看答案和解析>>
科目:高中化学 来源:2014届陕西省高二上学期期中考试化学试卷(解析版) 题型:选择题
对1L 1mol·L-1的NH4Cl溶液进行如下操作,溶液的pH增大的是( )
A.加热 B.加水稀释
C.加入少量的NH4Cl固体 D.再加1L 1mol·L NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com