
| A. | H2SO3+ClO-→2 H++SO42-+Cl- | B. | SO2+ClO-+H2O→2 H++SO42-+Cl- | ||
| C. | SO2+ClO-+H2O→SO32-+HClO | D. | SO2+ClO-+2OH-→SO42-+Cl-+H2O |
分析 二氧化硫少量,所有的二氧化硫都完全被氧化成SO42-,84消毒液的溶质为NaClO,次氯酸钠在反应后被还原成Cl-,利用电子守恒、质量守恒定律配平即可.
解答 解:少量SO2通入“84消毒液”中,SO2完全被氧化成SO42-,化合价升高(6-4)=2价,
84消毒液的溶质为NaClO,次氯酸钠在反应后被还原成Cl-,化合价变化为2,
则化合价变化的最小公倍数为2,反应中二氧化硫与次氯酸根离子的计量数相等,都是1,结合质量守恒配平该反应的离子方程式为:SO2+ClO-+2OH-→SO42-+Cl-+H2O,
故选D.
点评 本题考查了氧化还原反应的配平、离子方程式书写,题目难度中等,明确氧化还原反应的特征为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
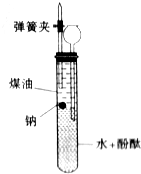 (1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.
(1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于m mL | B. | 等于m mL | C. | 大于m mL | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验内容 | 试剂 | 实验现象 |
| 验证氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | 有关信息 |
| X | 最高价氧化物对应的水化物能与其气态氢化物反应生成盐 |
| Y | M层上有3个电子 |
| Z | 短周期元素中原子半径最大的主族元素 |
| W | 其单质是淡黄色固体 |
| Q | 最高正价与最低负价代数和为6 |
| A. | 简单离子的半径大小顺序为:W>Q>Z>Y | |
| B. | W单质在氧气中燃烧后的产物不能使品红溶液褪色 | |
| C. | X、W和氢三种元素形成的化合物中只有共价键 | |
| D. | Z与W元素只能形成原子个数比为2:1的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com