


科目:高中化学 来源: 题型:
 美丽的“水立方”(Water Cube)是北京奥运会游泳馆,设计灵感来自于有机细胞的天然图案以及肥皂泡的形成.在这个中心的蓝色汽泡墙之内,钢结构的基本单位是一个由 12 个正五边形和2个正六边形所组成的几何细胞.覆盖这个框架的是半透明的汽泡,称为PTFE膜(聚四氟乙烯),它能为场馆内带来更多的自然光.根据以上信息,下列说法不正确的是( )
美丽的“水立方”(Water Cube)是北京奥运会游泳馆,设计灵感来自于有机细胞的天然图案以及肥皂泡的形成.在这个中心的蓝色汽泡墙之内,钢结构的基本单位是一个由 12 个正五边形和2个正六边形所组成的几何细胞.覆盖这个框架的是半透明的汽泡,称为PTFE膜(聚四氟乙烯),它能为场馆内带来更多的自然光.根据以上信息,下列说法不正确的是( )| A、若设想将一个结构单元钢棍焊成足球形状“碳笼”,它与C24形状相似 |
| B、若设想将一个结构单元钢棍焊成足球形状“碳笼”,需钢棍(相当于键)36 根 |
| C、PTFE的单体为:CF2=CF2 |
| D、PTFE在空气中易被氧气氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
12 6 |
 ⑨
⑨13 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
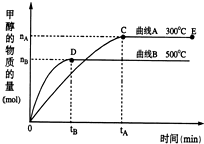 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com