
(10)光催化制氢是化学研究的热点之一。科学家利用含有呲啶环(呲啶的结构式为![]() ,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):
,其性质类似于苯)的化合物II作为中间体,实现了循环法制氢,示意图如下(仅列出部分反应条件):

(1)化合物II的分子式为______________。
(2)化合物I合成方法如下(反应条件略,除化合物III的结构未标明外,反应式已配平);
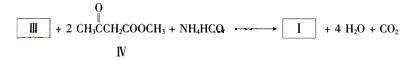
 化合物III的名称是________________。
化合物III的名称是________________。
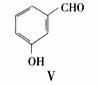
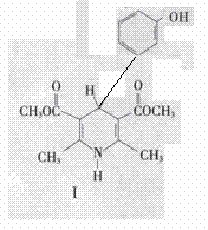
(3)用化合物V(结构式见右图)代替III作原料,也能进行类似的上述反应,所得有机产物的结构式为___________________。
(4)下列说法正确的是_____________(填字母)
A. 化合物V的名称是间羟基苯甲醛,或2-羟基苯甲醛
B. 化合物I具有还原性;II具有氧化性,但能被酸性高锰酸钾溶液氧化
C. 化合物I、II、IV都可发生水解反应
D. 化合物V遇三氯化铁显色,还可发生氧化反应,但不能发生还原反应
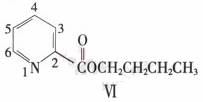 (5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为_________________;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有_________________种。
(5)呲啶甲酸酯可作为金属离子的萃取剂。2-呲啶甲酸正丁酯(VI)的结构式见右图,其合成原料2-呲啶甲酸的结构式为_________________;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体有_________________种。
(1)C11H13O4N
(2)甲醛
(3)
(4)B、C
(5) 12
12
解析:
(1)注意不要数掉了环上的氢原子,分子式为:C11H13NO4。
(2)因反应式已配平,故可依据原子守恒定律推知Ⅲ的分子式为CH2O,故为甲醛;(3)结合题(3)可以得到有机物的分子式为C(7+2×5+1-1)H(6+2×8+5-8)O(2+2×3+3―4×1―2)N,所得化合物与化合物I相比多出部分为C6H4NO,由此可以确定甲醛在反应中提供化合物ICH2部分,化合物V应该提供 部分替代CH2部分,所以所得化合物的结构式;
部分替代CH2部分,所以所得化合物的结构式;
(4)系统命名法Ⅴ的名称为3-羟基苯甲醛,A错,有机物Ⅴ含有的官能团为酚羟基和醛基,能发生显色反应即氧化反应,醛基和苯环均能与氢气发生加成反应(还原反应),D错;同理Ⅱ能加氢发生还原反应,具有氧化性,而其侧链甲基类似于苯的同系物的性质能被高锰酸钾溶液硬化,B正确,I、Ⅱ、Ⅳ分子内都有酯基,能够发生水解,C正确;
(5)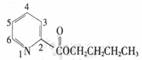 水解生成2―呲啶甲酸和丁醇,结合酯的水解反应我们不难得到2―呲啶甲酸的结构式为:
水解生成2―呲啶甲酸和丁醇,结合酯的水解反应我们不难得到2―呲啶甲酸的结构式为:![]() ;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体种类强调的是其同分异构体中,而不是VI中呲啶环上只有一个氢原子被取代异构体种类。注意这点就不会出错了。
;VI的同分异构体中,呲啶环上只有一个氢原子被取代的呲啶甲酸酯类同分异构体种类强调的是其同分异构体中,而不是VI中呲啶环上只有一个氢原子被取代异构体种类。注意这点就不会出错了。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:模拟题 题型:填空题
 CaCO3
CaCO3  2MgO+C
2MgO+C 
 CH3OH(g)。某研究小组将2 mol
CH3OH(g)。某研究小组将2 mol 
查看答案和解析>>
科目:高中化学 来源: 题型:
(06年江苏卷)(10分)利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如右图所示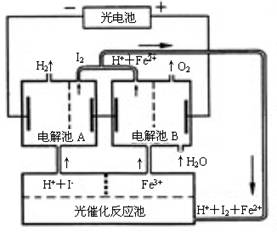 的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。
的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。
⑴写出电解池A、电解池B和光催化反应池中反应的离子方程式。
⑵若电解池A中生成3.36 L H2(标准状况),试计算电解池B中生成Fe2+的物质的量。
⑶若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol?L-1和b mol?L-1,光催化反应生成Fe3+的速率为c mol?L-1,循环系统中溶液的流量为Q(流量为单位时间内流过的溶液体积)。试用含所给字母的代数式表示溶液的流量Q。
查看答案和解析>>
科目:高中化学 来源: 题型:
(06年江苏卷)(10分)利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如右图所示 的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。
的循环系统实现光分解水制氢。反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用。
⑴写出电解池A、电解池B和光催化反应池中反应的离子方程式。
⑵若电解池A中生成3.36 L H2(标准状况),试计算电解池B中生成Fe2+的物质的量。
⑶若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol?L-1和b mol?L-1,光催化反应生成Fe3+的速率为c mol?L-1,循环系统中溶液的流量为Q(流量为单位时间内流过的溶液体积)。试用含所给字母的代数式表示溶液的流量Q。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com