
【题目】在制电路板时常用氯化铁溶液作为“腐蚀液”。发生反应的化学方程式如下2FeCl3+Cu=2FeCl2+CuCl2,下列有关说法正确的是( )
A.该化学反应属于置换反应B.该化学反应中FeCl3作还原剂
C.反应中Cu失去电子D.反应过程中所有元素的化合价都发生了变化
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应2SO2+O2![]() 2SO3,反应达平衡的标志是
2SO3,反应达平衡的标志是
①单位时间内消耗2 mol SO2的同时生成2 mol SO3
②反应混合物中,SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
A. ①②B. ①③C. ①D. ③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应中,氧化反应与还原反应在同种元素中进行的是
A.Cl2+2NaOH===NaCl+NaClO+H2O
B.2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
C.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)![]() CH3OH(g) △H<0,在容积为1 L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法不正确的是( )
CH3OH(g) △H<0,在容积为1 L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法不正确的是( )
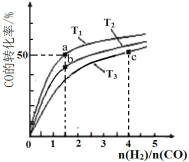
A. H2转化率:a>b>c
B. 上述三种温度之间关系为T1>T2>T3
C. a点状态下再通入0.5 mol CO和0.5 molCH3OH,平衡不移动
D. c点状态下再通入1 molCO和4 mol H2,新平衡中H2的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在同温同压下,相等质量的氧气和臭氧,它们的物质的量之比为_____,分子个数比为_____,原子个数比为_____。
(2)在一密闭容器中充入a mol NO 和b mol O2,可发生如下反应:2NO+O2═2NO2,充分反应后容器中氮原子和氧原子的个数之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池是一种化学电源,以Mg和石墨为电极,海水为电解质溶液,示意图如下。下列说法不正确的是

A. 石墨电极是该电池的正极
B. 石墨电极上发生还原反应
C. Mg电极的电极反应式:Mg-2e-=Mg2+
D. 电池工作时,电子从Mg电极经导线流向石墨电极,再从石墨电极经电解质溶液流向Mg电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A为气体化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。若甲为淡黄色固体,D和A的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。

则(1)A的分子式是______________,甲的电子式是______________。
(2)D的溶液与乙反应的离子方程式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.只含有一种元素的物质一定是纯净物
B.石墨在一定条件下转变为金刚石是化学变化
C.有单质参加的反应一定是氧化还原反应
D.碳元素只能形成金刚石和石墨两种同素异形体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com