
����Ŀ����ѧ�����ǵġ���ʳס�С���������أ�
��1���ٲ��������������������Ҫ���ʻ������Ͻ��DZ��㷺Ӧ�õĽ������ϣ������� ������Ͻ𡱻����Ͻ𡱣�������ʴ��Ҫ�������ǵ绯ѧ��ʴ���为����ӦʽΪ �����ǽ������ϰ���������ˮ��� ��
����˿֯Ʒ�뻯��֯Ʒ����������õ����ϣ������й�˵������ȷ���� ��
A����˿֯Ʒ����Ҫ����C��H��O��N����Ԫ��
B��������ȼ�յķ���������
C������֯Ʒ�гɷ������ؽ����Σ�ǿ�ᣬǿ��л���Ȼ����������ʧȥ����
D�����ֲ�Ʒ�����ڸ߷��Ӳ���
��2�����ҹ�����һ����Һƫ���ԣ�ƽʱ��ʳ��Ӧ��� ������ࡱ����������������ˮ�������ȼ���ʳ���Ԫ�������彡��������أ�Ϊ��Ԥ����ȱ���������ˡ�ʳ�μӵ⡱��������ʳ���м������� ��������ȱ����ƶѪ�ɷ��á������衱���ں���FeSO4���������һ�����£��������ʵ���жϸ��������Ƿ��� ��
�ڷ�ҩʱҪ��֢��ҩ��θ��ƽ����Ҫ�ɷ�Al��OH��3������������ �����ð���ȡ�����ϸ����Ⱦ������θ����ࡱ����������ʹҩ��˾ƥ�ֵĽṹʽΪ![]()
����д�����к��е�һ�������ŵ����� ��
��3��������β������Ҫ��NO�����ʣ��dz��е���ȾԴ�������ķ���֮һ������������������װһ������ת���������ò����ٺϽ����������������ص���ʹCO��NO��Ӧ�����������壮д��CO��NO��Ӧ�Ļ�ѧ����ʽ�� ��
�ڻ�ýྻ��ȫ������ˮ��ÿ���˵�������Ҫ��ijũ�����Ϊ�������ˮ���ڽ��ر�ˮȡ�ؼҺ�ʹ��Ư�۽���ɱ����������ԭ�����û�ѧ����ʽ��ʾΪ ��
�۰����ڼ�ʹ����ȫ���オ�����ϴ������ڲ����ʹ��������������ô�ͳ�ĸ߷��Ӳ��Ͼ���ϩ��������ϩ���۱���ϩ�ȣ�����Ϊ�˷�ֹ ����д��������������������ڣ�������λϯ��ͨ��������ר�������䣬�����Ϸֱ�����ɫ�ͺ�ɫ�������С��ɻ�����͡���������������ͼͼ���ʾ ��

���𰸡���1�������Ͻ�Fe��2e��=Fe2+���մɣ�
��C��
��2����ˮ��������أ���ȥҩƬ�ϵ����£���ҩƬ���飬�����ձ��У��ܽ⣬���˺�����Һ�м���������أ������Һ���ɫ��˵���Ѿ����ʣ������Һû���ɫ˵��û���ʣ�
��θ����ࣻ�Ȼ���
��3����2CO+2NO![]() 2CO2+N2��
2CO2+N2��
��Ca��ClO��2+CO2+H2O=CaCO3��+2HClO��
�۰�ɫ��Ⱦ���ɻ����
��������
�����������1���ٸ�������̼�ĺϽ�����ʴ��Ҫ�������ǵ绯ѧ��ʴ���为������������Ӧ��ʧȥ�������ɶ��������ӣ����ǽ�����������ijЩԪ�ص������̼��������±�ػ���������Լ������Ρ������Ρ������Ρ������ε�������ɵIJ��ϣ��������в�����ˮ�ࡢ�մɵȣ�
��������˿֯Ʒ�ɷ�Ϊ�����ʣ�����֯Ʒ�Dz����Ӵ���Ȼ��ά���ϣ������ɵ��ڡ����ڡ����ڡ����ڡ�ά�ڡ����ڡ�ճ����������������ά����˿�Ȳ����е�һ�ֻ��ֺϳɵIJ����Ƴɵ���������������жϽ��
��2���ٺ��ء��ơ��ơ�þ�ȿ����ʽ϶��ʳ������ڵ����յĴ�л���ﳣ�ʼ��ԣ������������ʵij�Ϊ����ʳƷ���߲ˡ�ˮ�������ࡢ�;���ʳ��ȣ��ӵ��������ӵ�Ϊ����أ������������������������������������ӣ������������������������Ѫ��ɫ��
�����������ܹ������ᷴӦ���������ӣ�![]() �����Ȼ���������
�����Ȼ���������
��3����CO��NO�ڴ������������ɵ����Ͷ�����̼��
��Ư��������Ӵ���Ͷ�����̼ˮ��Ӧ����̼��ƺʹ����ᣬ���������ǿ�����ԣ��ܽ���ɱ������Ư�ף�
��ѡ���ܹ���������ϴ���Ϊ�˷�ֹ���ܽ���������Ļ�����Ⱦ����������Ϊ�ɻ�����Ͳ��ɻ����
�⣺��1���ٸ�������̼�ĺϽ�
����ʴ��Ҫ�������ǵ绯ѧ��ʴ���为������������Ӧ��ʧȥ�������ɶ��������ӣ��缫��ӦʽΪ��Fe��2e��=Fe2+��
�������в�����ˮ�ࡢ�մɵȣ�
�ʴ�Ϊ�����Ͻ�Fe��2e��=Fe2+���մɣ�
��A����˿֯Ʒ��Ҫ�ɷ�Ϊ�����ʣ���Ҫ����C��H��O��N����Ԫ�أ���A��ȷ��
B����˿��Ʒ���е��������ղ����ս���ë����ζ������֯Ʒ�����д����ʣ���B��ȷ��
C����˿֯Ʒ�гɷ������ؽ����Σ�ǿ�ᣬǿ��л���Ȼ����������ʧȥ���ԣ�����֯Ʒ���������ʲ����д����ʣ���C����
D�����ֲ�Ʒ�����ڸ߷��Ӳ��ϣ���D��ȷ��
��ѡ��C��
��2����ˮ��Ϊ����ʳ��ӵ�����ָ��ʳ���м������ĵ���أ������������������������������������ӣ������������������������Ѫ��ɫ�����Լ����������Ƿ���ʷ�������ȥҩƬ�ϵ����£���ҩƬ���飬�����ձ��У��ܽ⣬���˺�����Һ�м���������أ������Һ���ɫ��˵���Ѿ����ʣ������Һû���ɫ˵��û���ʣ�
�ʴ�Ϊ��ˮ��������أ���ȥҩƬ�ϵ����£���ҩƬ���飬�����ձ��У��ܽ⣬���˺�����Һ�м���������أ������Һ���ɫ��˵���Ѿ����ʣ������Һû���ɫ˵��û���ʣ�
�����������ܹ������ᷴӦ���������ӣ����Կ�����������θ����ࣻ![]() �����Ȼ���������
�����Ȼ���������
�ʴ�Ϊ��θ����ࣻ�Ȼ���
��3����CO��NO�ڴ������������ɵ����Ͷ�����̼������ʽ��2CO+2NO![]() 2CO2+N2��
2CO2+N2��
�ʴ�Ϊ��2CO+2NO![]() 2CO2+N2��
2CO2+N2��
��̼������ǿ�ڴ����ᣬƯ��������Ӵ���Ͷ�����̼ˮ��Ӧ����̼��ƺʹ����ᣬ���������ǿ�����ԣ��ܽ���ɱ������Ư�ף���Ӧ�Ļ�ѧ����ʽΪ��Ca��ClO��2+CO2+H2O=CaCO3��+2HClO��
�ʴ�Ϊ��Ca��ClO��2+CO2+H2O=CaCO3��+2HClO��
�����ϲ����⣬Ӱ�컷�������ۣ������ɷ���DZ��Σ��������������װ���϶�Ϊ��ɫ��������Ϊ��ɫ��Ⱦ���ɻ���������ظ����ã�����ѭ��ͼ�꣬
�ʴ�Ϊ����ɫ��Ⱦ���ɻ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����е����ʾ��ܷ����ӳɷ�Ӧ����(����)
A. ��ϩ���Ҵ� B. ��������ϩ
C. ����������� D. ��ϩ�ͱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ�϶���ʹ��ѧ��Ӧ�����������( )
A������Ӧ����� B������ѹǿ C�������¶� D��ʹ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(16�֣�25��ʱ���������ʵĵ���ƽ�ⳣ�������ʾ��
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.7��10-5 | K1=4.3��10-7 K2=5.6��10-11 | 3.0��10-8 |
��ش��������⣺
��1��CH3COOH��H2CO3��HClO��������ǿ������˳��Ϊ__________��
��2��ͬŨ��CH3COO-��HCO3-��CO32-��ClO-���H+��������ǿ������˳��Ϊ__________��
��3��������CO2����ͨ��NaClO��Һ�У�д����Ӧ�����ӷ���ʽ��_______��
��4��������0.1 mol��L-1��CH3COOH��Һ�ڼ�ˮϡ�����У���д���б���ʽ�е����ݱ仯���(���������������С������������)
��![]() ______����
______����![]() ______��
______��
��![]() _______����
_______����![]() _______��
_______��
��5�����Ϊ10mLpH=2�Ĵ�����Һ��һԪ��HX�ֱ��ˮϡ����1000mL��ϡ������pH�仯��ͼ��ʾ����HX�ĵ���ƽ�ⳣ��______(������������������������С����)����ĵ���ƽ�ⳣ����������______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������мס��ҡ�����ͼ���ж�������������ȷ���ǣ� ��
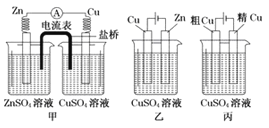
A. ����ԭ��أ����ǵ��װ�� B. �ס���װ���У�п���Ͼ�����������Ӧ
C. �ҡ���װ���У�����������������Ӧ���ܽ� D. ��װ���У�ͭ�缫�����������м�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѡ��3�������ʽṹ������]
X��Y��Z��W��Q��R��Ϊǰ������Ԫ�أ���ԭ���������������������Ϣ���±���ʾ��
XԪ�صĻ�̬ԭ���е��ӷֲ���������ͬ���ܼ��У���ÿ���ܼ��еĵ���������ͬ |
YԪ�ص���̬�⻯����������������Ӧ��ˮ�����ܷ������Ϸ�Ӧ |
ZԪ�ص����������������������� |
Wԭ�ӵĵ�һ�����������ֱܷ�Ϊ�� I1=578KJ��mol-1 I2=1817KJ��mol-1 I3=2745KJ��mol-1 I4=11575KJ��mol-1 I5=14830KJ��mol-1 I6=18376KJ��mol-1 |
QΪǰ�������е縺����С��Ԫ�� |
Ԫ��Rλ�����ڱ��ĵ�10�� |
�ش��������⣺
(1)YԪ�صĻ�̬ԭ�ӵĵ����Ų�ʽΪ_____________,���һ�����ܱ�ZԪ��ԭ�ӵĵ�һ������________(��ߡ��͡�)
(2)X���Ȼ�����۵��Q���Ȼ�����۵�_______________(��ߡ��͡�)��������___________________
(3)����֤ʵԪ��W�ĵ�����ǿ������Һ��Ӧ��W(OH)4]-���ɣ���W(OH)4]-�д���_______(����ĸ)
a�����Թ��ۼ� b���Ǽ��Թ��ۼ� c����λ�� d�����
(4)����X��R��þ����Ԫ�ص�ij�־�����г����ԣ���ṹ����ͼ��ʾ����þ���Ļ�ѧʽΪ_________��������ÿ��þԭ����Χ���������Rԭ����___________����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ɱ���ϩ�Ƶõľ۱���ϩ����������һ���Բ;ߣ�![]()
��1������ϩ�ķ���ʽΪ ��
��2������ϩ��ȡ�۱���ϩ�Ļ�ѧ����ʽΪ ��
�۱���ϩ���������ȶ�����������صġ���ɫ��Ⱦ����Ϊ�����ǿ�����һ�־���������������۱���ϩ��������ϳɹ������£�

��3�����ۺ���ά�صķ���ʽ���ɱ�ʾΪ��C6H10O5��n�����й��ڵ��ۺ���ά�ص�˵����ȷ����
A����Ϊͬ���칹�� B��ˮ�����ղ�����ͬ
C����ά���Ǵ����� D�����Ǹ߷��ӻ�����
��4����������������������� �������ƣ���
��5�����ݽṹ�ƶϾ�������ܷ����ķ�Ӧ������ �����ݴ�˵���þ�������������۱���ϩ���ϵĺô��� ��
��6������������Na��Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��һ��������ɰֽ��ϸ��ĥ����ȥ����ı���Ĥ��������ǯ��ס���ھƾ��ƻ����ϼ��ȣ��۲쵽��������( )
A. ����ȼ�� B. ����ҫ�۰� C. �ۻ��������� D. ʧȥ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������11�����Ӻ�10�����ӵ�������
A. Na�� B. O2�D C. Mg2�� D. F�D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com