
【题目】(16分)25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为__________。
(2)同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为__________。
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:_______。
(4)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,填写下列表达式中的数据变化情况(填“变大”、“变小”或“不变”)
①![]() ______;②
______;②![]() ______;
______;
③![]() _______;④
_______;④![]() _______。
_______。
(5)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数______(填“大于”、“等于”或“小于”)醋酸的电离平衡常数:理由是______。

【答案】(1)CH3COOH>H2CO3>HClO;
(2)CO32->ClO->HCO3->CH3COO-;
(3)CO2+H2O+ClO-=HClO+HCO3-;
(4)①变小;②不变;③变大;④不变;
(5)>;当完全电离时应该是PH=4,现在PH值HX>CH3COOH,说明原来HX电离更多,故HX的电离平衡常数>醋酸的电离平衡常数。
【解析】
试题分析:(1)酸电离程度越大,其在相同温度下的电离平衡常数就越大,根据表格数据可知电离平衡常数CH3COOH>H2CO3>HClO,所以酸性:CH3COOH>H2CO3>HClO;(2)同浓度的酸的酸性越强,其电离平衡常数越大,电离产生的酸根离子结合氢离子的能力就越弱。由于电离平衡常数: K(CH3COOH)>K(H2CO3)>K(HCO3-)>K(HClO),所以CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-;(3)由于电离平衡常数:K(H2CO3)>K(HCO3-)>K(HClO),所以将少量CO2气体通入NaClO溶液中,反应的离子方程式:CO2+H2O+ ClO-=HClO+ HCO3-;(4)在常温下,醋酸在溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,①溶液在加水稀释过程中,c(CH3COOH)、c(H+)由于稀释都减小,同时电离平衡正向移动,使溶液中
CH3COO-+H+,①溶液在加水稀释过程中,c(CH3COOH)、c(H+)由于稀释都减小,同时电离平衡正向移动,使溶液中![]() 减小;②
减小;②![]() =
=![]() ,电离平衡常数只与温度有关,温度不变,电离平衡常数不变;③在溶液的稀释时,c(CH3COOH)、c(CH3COO-)都减小,电离平衡正向移动,使c(CH3COOH)进一步减小,c(CH3COO-)又有所增大,所以
,电离平衡常数只与温度有关,温度不变,电离平衡常数不变;③在溶液的稀释时,c(CH3COOH)、c(CH3COO-)都减小,电离平衡正向移动,使c(CH3COOH)进一步减小,c(CH3COO-)又有所增大,所以![]() 增大;④
增大;④![]() =
=![]() ,由于在温度不变时,K、Kw都是常数,所以他们的比值不变;(5)根据图示可知:体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释了100倍,若HX是强酸,则其pH=4,实际pH<4,说明HX弱酸。酸电离程度越大,稀释时溶液中c(H+)变化越大,溶液的pH就越大,由于在稀释过程中pH变化HX>CH3COOH,则HX的电离平衡常数大于醋酸的电离平衡常数。
,由于在温度不变时,K、Kw都是常数,所以他们的比值不变;(5)根据图示可知:体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释了100倍,若HX是强酸,则其pH=4,实际pH<4,说明HX弱酸。酸电离程度越大,稀释时溶液中c(H+)变化越大,溶液的pH就越大,由于在稀释过程中pH变化HX>CH3COOH,则HX的电离平衡常数大于醋酸的电离平衡常数。


科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述正确的是( )
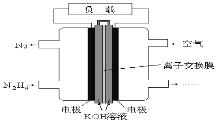
A.电子从右侧电极经过负载后流向左侧电极
B.负极发生的电极反应式为:N2H4 - 4e-=N2+4H+
C.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D.该燃料电池持续放电时.K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )

A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C. 离子Y2﹣和Z3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①能量越低的物质就越稳定,②白磷转化成红磷是放热反应。据此,下列判断或说法中正确的是( )
A.在相同的条件下,红磷比白磷能量高
B.在相同的条件下,白磷比红磷稳定
C.红磷和白磷的结构不同
D.红磷容易发生自燃而白磷则不会自燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是( )
A. S2﹣离子的结构示意图:![]()
B. H2O2的电子式:![]()
C. CO2的比例模型:![]()
D. 有8个质子、10个中子的核素:188O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H都是中学化学中常见的物质,其中,常温下A能使铁或铝钝化,B是固体非金属单质,C为水,D是一种能使品红溶液褪色的无色气体,F是金属单质,G可以用作耐火材料,它们之间有如下转化关系.

(1)写出下列物质的化学式:E ,H .
(2)写出A溶液与B反应的化学方程式: .
试写出E与F的反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人们的“衣食住行“,休戚相关.
(1)①材料是人类赖以生存的重要物质基础.合金是被广泛应用的金属材料.钢属于 (填“铁合金”或“铝合金”);铁锈蚀主要发生的是电化学腐蚀,其负极反应式为 ;无机非金属材料包括玻璃、水泥和 .
②真丝织品与化纤织品是生活中最常用的面料,下列有关说法不正确的是 .
A.真丝织品中主要含有C,H,O,N四种元素
B.可以用燃烧的方法来区分
C.化纤织品中成分遇到重金属盐,强酸,强碱,有机物等会产生沉淀而失去活性
D.两种产品都属于高分子材料
(2)①我国居民一般尿液偏酸性,平时饮食中应多吃 (填”肉类”,”几鸡蛋”,”水果”)等碱性食物;微量元素与人体健康密切相关,为了预防碘缺乏,启动了”食盐加碘”,就是在食盐中加适量的 .如治疗缺铁性贫血可服用”亚铁丸”(内含有FeSO4,外面裹了一层糖衣),试设计实验判断该亚铁丸是否质 .
②服药时要对症下药,胃舒平(主要成分Al(OH)3)适用于治疗 (填”感冒发热”,”细菌感染”,”胃酸过多”).解热镇痛药阿司匹林的结构式为![]()
请你写出其中含有的一个官能团的名称 .
(3)①汽车尾气(主要有NO等物质)是城市的污染源.治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂.钯合金作催化剂).它的特点是使CO与NO反应,生成无毒气体.写出CO与NO反应的化学方程式: .
②获得洁净安全的饮用水是每个人的正常需要.某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉进行杀菌消毒,其原理可用化学方程式表示为 .
③奥运期间使用了全生物降解塑料袋,用于餐饮和处理垃圾,而不用传统的高分子材料聚乙烯、聚氯乙烯及聚苯乙烯等,这是为了防止 (填写环境术语).“鸟巢”体育场内,各区座位席的通道口设有专门垃圾箱,箱体上分别用绿色和黑色字样标有“可回收物”和“其他垃圾”,如图图标表示 .

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某些气态烃可以在氯气中燃烧,如:CH4+2Cl2![]() C+4HCl,现将一定量的某烃分成两等份,分别在氯气和氧气中燃烧,测得消耗的氯气和氧气在同温同压下的体积比为3:3.5,则该烃的分子式为( )
C+4HCl,现将一定量的某烃分成两等份,分别在氯气和氧气中燃烧,测得消耗的氯气和氧气在同温同压下的体积比为3:3.5,则该烃的分子式为( )
A. C2H4 B. C2H6 C. C3H6 D. C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别燃烧等物质的量的下列各组物质,其中消耗氧气的量相等的是( )
①C2H2与C2H4O ②C4H8与C6H12O6 ③C7H8与C6H12 ④HCOOCH3与CH3COOH.
A.①③④ B.①②③④ C.①④ D.①②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com