
【题目】分别燃烧等物质的量的下列各组物质,其中消耗氧气的量相等的是( )
①C2H2与C2H4O ②C4H8与C6H12O6 ③C7H8与C6H12 ④HCOOCH3与CH3COOH.
A.①③④ B.①②③④ C.①④ D.①②④
【答案】B
【解析】
试题分析:设所给物质的通式为CxHyOz,则其燃烧方程式为:CxHyOz+(x+![]() ﹣
﹣![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O,所以1mol物质消耗氧气的量多少取决于(x+
H2O,所以1mol物质消耗氧气的量多少取决于(x+![]() ﹣
﹣![]() ),据此解答.
),据此解答.
解:①1molC2H2 完全燃烧消耗氧气的物质的量为2+![]() =2.5;1molC2H4O完全燃烧消耗氧气的物质的量为2+
=2.5;1molC2H4O完全燃烧消耗氧气的物质的量为2+![]() ﹣
﹣![]() =2.5,二者相等,故选;
=2.5,二者相等,故选;
②1moC4H8完全燃烧消耗氧气的物质的量为4+![]() =6;与C6H12O6完全燃烧消耗氧气的物质的量为6+
=6;与C6H12O6完全燃烧消耗氧气的物质的量为6+![]() ﹣
﹣![]() =6,二者相等,故选;
=6,二者相等,故选;
③1moC7H8完全燃烧消耗氧气的物质的量为7+![]() =9;与1molC6H12完全燃烧消耗氧气的物质的量为6+
=9;与1molC6H12完全燃烧消耗氧气的物质的量为6+![]() =9,二者相等,故选;
=9,二者相等,故选;
④HCOOCH3与CH3COOH互为同分异构体,1mol完全燃烧耗氧量相等,故选;
故选:B.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】(16分)25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为__________。
(2)同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为__________。
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:_______。
(4)常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,填写下列表达式中的数据变化情况(填“变大”、“变小”或“不变”)
①![]() ______;②
______;②![]() ______;
______;
③![]() _______;④
_______;④![]() _______。
_______。
(5)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数______(填“大于”、“等于”或“小于”)醋酸的电离平衡常数:理由是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学将一块铝箔用砂纸仔细打磨,除去表面的保护膜,用坩埚钳夹住放在酒精灯火焰上加热,观察到的现象是( )
A. 剧烈燃烧 B. 发出耀眼白光 C. 熔化的铝滴落 D. 失去金属光泽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下,回答下列问题:
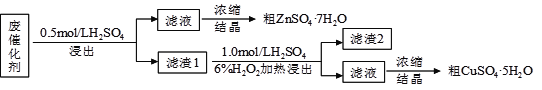
已知:ZnS与稀硫酸反应,且化合价不变; CuS既不溶解于稀硫酸,也不与稀硫酸反应
(1)在下列装置中,第一次浸出反应装置最合理的___________(填标号)。

(2)滤液1中含有Fe2+,选用提供的试剂进行检验,检验方法如下: 。
(提供的试剂:稀盐酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水)
(3)本实验要用到抽滤,设所用的洗涤剂为X,抽滤洗涤沉淀的操作 。
(4)写出第二次浸出的化学反应方程式 ,向盛有滤渣1的反应器中加H2SO4和H2O2溶液,应先加 。
(5)滤渣2的主要成分是 。浓缩、结晶得到硫酸锌晶体的主要仪器名称是 。
(6)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中不正确的是( )
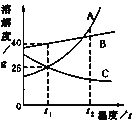
A.t1℃时,B物质的溶解度为40g
B.要将C的不饱和溶液转化为饱和溶液可以采取降温的方法
C.t2℃时,三种物质的溶解度由大到小的顺序为:A>B>C
D.将t2℃时A、B的饱和溶液降温到t1℃时,析出的晶体A比B多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛋白质是由多种氨基酸构成的极为复杂的化合物,相对分子质量从几万到几百万。下图为丙氨酸分子结构模型,下列关于丙氨酸的说法正确的是

A.它是由四种元素组成的有机高分子化合物
B.每个丙氨酸分子中含有13个原子核
C.丙氨酸分子中含有3个碳原子
D.丙氨酸分子中氮、氧元素的质量比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四个反应,其焓变和熵变如下表所示
反应 | A | B | C | D |
ΔH/kJ·mol-1 | 10.5 | 1.80 | -126 | -11.7 |
ΔS/J·mol-l·K -1 | 30.0 | -113.0 | 84.0 | -105.0 |
(1)在任何温度都能自发进行的反应是________;任何温度下都不能自发进行的反应是________。
(2)高温才可以自发进行的反应是________;低温有利于自发进行的反应是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲将氯化钠、沙子(主要成分为SiO2)、碘三种物质组成的固体混合物分离,最科学的操作顺序是( )
A.溶解、过滤、加热(升华)、蒸发(结晶)
B.加热(升华)、溶解、过滤、蒸发(结晶)
C.加热(升华)、溶解、蒸馏、结晶
D.溶解、结晶、过滤、加热(升华)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com