
���� ��1�����������ã������ᷴӦ���ң������Ȼ�����������
��2��������ϡ���ᷴӦ��ȡ����ʱ�����������ӵ�Ũ�ȡ������¶ȡ�����Ӵ�����ȿɼӿ췴Ӧ���ʣ��Դ������
��� �⣺��1�����������ã������ᷴӦ���ң������Ȼ�������������Ӧ�����ӷ���ʽΪ���ʴ�Ϊ������2Al+6H+=2Al3++3H2����
��2���ٸijɵ�Ũ�ȵ�ϡ���ᣬ������Ũ������Ӧ�������ʴ�Ϊ������
�������ˮϡ�ͣ�Ũ�ȼ�С����Ӧ���ʼ�С���ʴ�Ϊ����С��
�����Լ������ᣬ�¶����ߣ���Ӧ�������ʴ�Ϊ������
�ܼ�����������NaCl����Ũ����Ӱ�죬��Ӧ���ʲ��䣬�ʴ�Ϊ�����䣻
���ټ���������ͬ��Al�ۣ�Ũ�Ȳ��䣬���ʲ��䣬�ʴ�Ϊ�����䣻
��ͨ������HCl���壬Ũ������Ӧ�������ʴ�Ϊ������
���� ���⿼��Ӱ�컯ѧ��Ӧ���ʵ����أ�Ϊ��Ƶ���㣬��ȷ�¶ȡ�Ũ�ȡ������Է�Ӧ��Ӱ�켴�ɽ��ע�ػ���֪ʶ�Ŀ��飬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
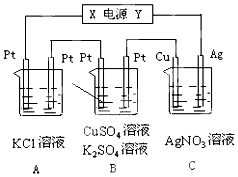 ��ͼ��ʾ����Һ�����Ϊ200mL�������5minʱͭ�缫��������2.16g���Իش�
��ͼ��ʾ����Һ�����Ϊ200mL�������5minʱͭ�缫��������2.16g���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͬ���� | B�� | ��ͬ���� | ||
| C�� | ֻ�������������� | D�� | ֻ��ԭ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
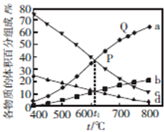 CO2��H2�ϳɼ��ѵ���Ҫ��Ӧ���£�
CO2��H2�ϳɼ��ѵ���Ҫ��Ӧ���£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 1000 | 1115 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | amol-1 | B�� | 2amol-1 | C�� | 4amol-1 | D�� | 8a mol-1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com