
科目:高中化学 来源: 题型:
| A、氨气通入醋酸溶液NH3+H+═NH4+ |
| B、金属钠跟水反应 2Na+2H2O═2Na++2OH-+H2↑ |
| C、铜与稀硝酸反应 Cu+2NO3-+2H+═Cu2++NO2↑+H2O |
| D、碳酸钙溶于盐酸 Ca2++2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向室内喷水,溶解液化石油气,防止其燃烧 |
| B、开灯,仔细检查泄漏源 |
| C、打开所有门窗通风,关闭气源阀门 |
| D、打电话报警,并请维修人员前来维修 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀盐酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B、氧化镁与稀硫酸混合:MgO+2H+=Mg2++H2O |
| C、铝片插入到硝酸银溶液中:Al+Ag+=Al3++Ag |
| D、稀盐酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)该有机化合物A用质谱仪测定时,测得分离出的最大的碎片的相对分子质量为90; | 试通过计算填空: (1)A的摩尔质量为: |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g; | (2)A的分子式为: |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)可推出A中含有的官能团:(写名称) |
(4)A的核磁共振氢谱如图: | (4)A中含有 |
| (5)综上所述,A的结构简式 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量晶体溶于适量蒸馏水中,用三支试管分别取上述溶液少许.用铂丝蘸取试管1中溶液进行 | 透过 | 结论:含有K+. |
| (2)向试管2中加入少量盐酸酸化,滴加少量 | 有白色沉淀. | 结论:含有 解释: (写离子方程式) |
| (3)向试管3中逐滴加入足量NaOH溶液,边加边振荡. | 结论:含有 解释: (写离子方程式) |
查看答案和解析>>
科目:高中化学 来源: 题型:
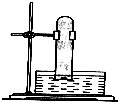 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请填写下列空白:
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请填写下列空白:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com