
【题目】阿司匹林的有效成分是乙酰水杨酸(![]() )。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
)。实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
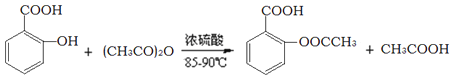
操作流程如下:
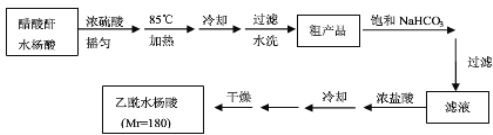
已知:水杨酸和乙酰水杨酸均微溶于水,但其钠盐易溶于水,醋酸酐遇水分解生成醋酸。
回答下列问题:
(1)合成过程中最合适的加热方法是______________。
(2)提纯粗产品流程如下,加热回流装置如图:
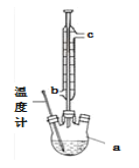
①沸石的作用是_______________;
②冷凝水的流出方向是____________(填“b”或“c”);
③使用温度计的目的是____________。
(3)检验最终产品中是否含有水杨酸的化学方法是_________________。
(4)阿司匹林药片中乙酰水杨酸含量的测定步骤(假定只含乙酰水杨酸和辅料,辅料不参与反应):
Ⅰ.称取阿司匹林样品m g;Ⅱ.将样品研碎,溶于V1 mL a mol·L-1NaOH(过量)并加热,除去辅料等不溶物,将所得溶液移入锥形瓶;Ⅲ.向锥形瓶中滴加几滴酚酞,用浓度为b mol·L-1的标准盐酸到滴定剩余的NaOH,消耗盐酸的体积为V2mL。
① 写出乙酰水杨酸与过量NaOH溶液加热发生反应的化学方程式______________。
② 阿司匹林药片中乙酰水杨酸质量分数的表达式为__________________。
【答案】水浴加热 防止暴沸 c 便于调控加热温度,防止乙酰水杨酸受热分解 取少量结晶于试管中,加蒸馏水溶解,滴加FeCl3溶液,若呈紫蓝色则含水杨酸 ![]() +3NaOH
+3NaOH![]() CH3COONa+2H2O+
CH3COONa+2H2O+![]()
![]() 或
或![]()
【解析】
醋酸酐和水杨酸混合,然后向混合溶液中加入浓硫酸,摇匀后加热至85℃,然后冷却、过滤、水洗得到粗产品,然后向粗产品中加入饱和碳酸氢钠溶液,使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,从而除去杂质;然后加入浓盐酸除去剩余的碳酸氢钠、将乙酰水杨酸钠转化为乙酰水杨酸,最后过滤、洗涤、干燥得到乙酰水杨酸.
(1)控制温度85℃,温度低于100℃,应采取水浴加热,受热均匀,便于控制温度,故答案为:水浴加热;
(2)根据提纯粗产品加热回流装置图可知:
①蒸馏烧瓶中加入沸石的作用是防止暴沸;②蒸馏时为了增强冷凝效果,冷凝水的流向应该与蒸汽的流向相反,故从c口进入,b口流出;③使用温度计的目的是控制温度,便于调控加热温度,防止乙酰水杨酸受热分解,故答案为:防止暴沸 c 便于调控加热温度,防止乙酰水杨酸受热分解;
(3)水杨酸含有羧基和酚羟基,而乙酰水杨酸中不含酚羟基,故检验最终产品中是否含有水杨酸的化学方法是检验酚羟基的方法,酚羟基能和氯化铁发生显色反应,检验最终产品中是否含有水杨酸的化学方法是:取少量结晶于试管中,加蒸馏水溶解,滴加FeCl3溶液,若呈紫色则含水杨酸;故答案为:取少量结晶于试管中,加蒸馏水溶解,滴加FeCl3溶液,若呈紫色则含水杨酸;
(4)①羧基能与氢氧化钠反应,水解得到的酚羟基、乙酸与氢氧化钠反应,故反应方程式为:![]() +3NaOH
+3NaOH![]() CH3COONa+2H2O+
CH3COONa+2H2O+![]() ,
,
故答案为:![]() +3NaOH
+3NaOH![]() CH3COONa+2H2O+
CH3COONa+2H2O+![]() ;
;
②乙酰水杨酸消耗的氢氧化钠的物质的量为:(aV1×10-3-bV2×10-3)mol,乙酰水杨酸的物质的量是消耗的氢氧化钠的物质的量的![]() ,阿司匹林药片中乙酰水杨酸质量分数的表达式为
,阿司匹林药片中乙酰水杨酸质量分数的表达式为
=![]() ,故答案为:
,故答案为:![]() 或
或![]() 。
。


科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家,磷酸铁锂锂离子电池充电时阳极反应式为,![]() ,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是
,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是
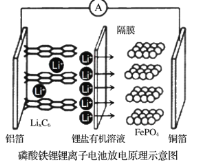
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:![]()
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在抗击新冠病毒肺炎中瑞德西韦是主要药物之一。瑞德西韦的结构如图所示,下列说法正确的是
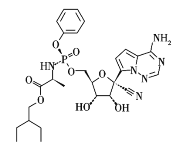
A.瑞德西韦中N、O、P元素的电负性:N>O>P
B.瑞德西韦中的O—H键的键能大于N—H键的键能
C.瑞德西韦中所有N都为sp3杂化
D.瑞德西韦结构中存在σ键、π键和大π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
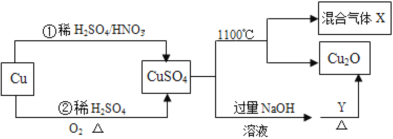
A.Y一定是葡萄糖溶液
B.相对于途径①,途径②更好地体现了绿色化学理念
C.混合气体X是只有SO2和SO3组成的混合气体
D.将CuSO4溶液蒸发浓缩、冷却结晶可制得硫酸铜晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】兴趣小组在实验室中模拟利用甲烷和氯气发生取代反应制取副产品盐酸,设计如图装置,下列说法错误的是( )
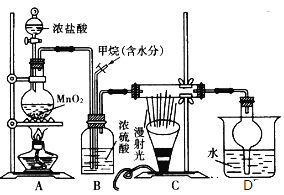
A.实验时先点燃A处酒精灯再通甲烷
B.装置B有均匀混合气体、控制气流速度、干燥混合气体等作用
C.从D中分离出盐酸的方法为过滤
D.装置C经过一段时间的强光照射后,生成的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
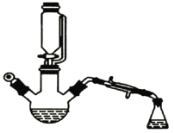
【题目】用下图所示装置制备乙酸乙酯粗产品(加热和夹持装置等省略),有关数据如下表所示:
物质 | C2H5OH | CH3COOH | CH3COOC2H5 |
密度g/cm3 | 0.79 | 1.05 | 0.90 |
沸点/℃ | 78.3 | 118 | 77.1 |
已知:乙醇可以和氯化钙反应生成微溶于水的CaC12·6C2H5OH。在三颈烧瓶内将过量的乙醇和少量的浓硫酸混合,然后经恒压分液斗边滴加酸,边加热蒸馏。得到含有乙醇、醋酸和水的乙酸乙酯粗产品。
(1)混合乙醇与浓硫酸时,应先加入的试剂是_______;浓硫酸的作用是__________。
(2)边滴加醋酸,边加热蒸馏的目的是_______。将粗产品再经下列步骤精制:
(3)为除去其中的醋酸,可向粗产品中加入______(填序号)。
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(4)向其中加入饱和氯化钙溶液。振荡、分离。其目的是______。
(5)然后再向其中加入无水硫酸钠,振荡,静置,以除去水分。最后,将经过上述处理后的液体放入一干燥的蒸馏烧瓶内。再蒸馏,弃去低沸点馏分,收集沸程76℃~____℃(填“78”或“118“)之间的馏分即得纯净的乙酸乙酯。
(6)在实验中原料用量:23.0mL乙醇、15.0mL冰醋酸,最终得到16.0mL乙酸乙酯,则本次实验中乙酸乙酯的产率为________(百分数精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室为探究铜与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法错误的是( )
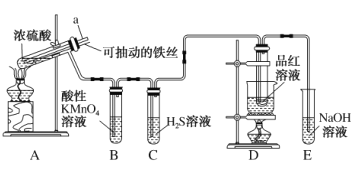
A.装置B、C的目的分别是验证二氧化硫的还原性、氧化性
B.实验结束后可向装置A的溶液中加水,以验证是否有蓝色溶液生成
C.装置D的目的是验证SO2的漂白性及漂白的不稳定性
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2)常用作种子及谷物的无毒性消毒剂,常温下为白色的固体,微溶于水,且不溶于乙醇、乙醚和碱性溶液,但溶于酸。某实验小组拟探究CaO2的性质及其实验室制法。
(1)实验探究CaO2与酸的反应。
操作 | 现象 |
向盛有4gCaO2的大试管中加入10mL稀盐酸得溶液a | 剧烈反应,产生能使带火星木条复燃的气体 |
取5mL溶液a置于试管中,滴入两滴石蕊溶液 | 溶液变红,一段时间后溶液颜色明显变浅,稍后溶液变为无色 |
①CaO2与盐酸反应的化学方程式为_____________。
②加入石蕊溶液后溶液褪色可能是因为溶液a中存在较多的_____________。
(2)用如图所示装置制备过氧化钙,其反应原理为Ca+O2![]() CaO2。
CaO2。
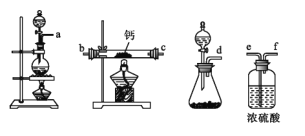
①请选择实验所需要的装置,按气流方向连接的顺序为_____________(填仪器接口的字母,上述装置可不选用也可重复使用)。
②根据完整的实验装置进行实验,实验步骤如下:Ⅰ.检验装置的气密性后,装入药品;Ⅱ.打开分液漏斗活塞,通入气体一段时间,加热药品;Ⅲ.反应结束后,_____________(填操作);Ⅳ.拆除装置,取出产物。
(3)利用反应Ca2++H2O2+2NH3+8H2O=CaO28H2O↓+2![]() 在碱性环境下制取CaO2的装置如图所示。
在碱性环境下制取CaO2的装置如图所示。
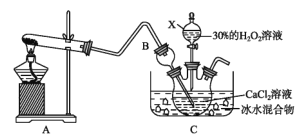
①NH3在Ca2+和H2O2的反应过程中所起的作用是_____________。
②反应结束后,经过滤、洗涤、低温烘干可获得CaO28H2O。过滤需要的玻璃仪器是_____________;将沉淀进行洗涤的操作为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学研究小组探究外界条件对化学反应mA(g)+nB(g)![]() pC(g)+qD(g)的速率和平衡的影响图像如下,下列判断错误的是( )
pC(g)+qD(g)的速率和平衡的影响图像如下,下列判断错误的是( )
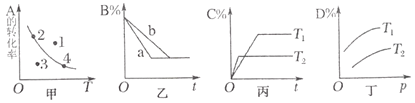
A.甲图中,表示反应速率v正>v逆的是点1
B.乙图中,若m+n=p+q,则a曲线可能使用了催化剂
C.由丙图可知,T1<T2,该反应正反应为放热反应
D.由丁图可知,该反应m+n>p+q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com