
| Kw |
| C(OH-) |
| 4×10-14 |
| 0.1 |
| 0.4mol/L+0.004mol/L |
| 2 |
| 3C-2C |
| 3+2 |
| C |
| 5 |
| Kw |
| C(H+) |
| 4×10-14 |
| 10-12 |
| C |
| 5 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、互为同系物的两种物质不可能互为同分异构体 |
| B、互为同分异构体的两种物质不可能互为同系物 |
| C、具有相同通式的有机物不一定互为同系物 |
| D、互为同分异构体的两种物质物理性质不同,但化学性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2S(g)+O2(g)=2S (s)+2H2O(l)△H=-Q2 kJ/mol | ||
| B、CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-802.3kJ/mol | ||
C、CO(g)+
| ||
| D、2H2(g)+O2(g)═2H2O(1);△H=-571.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
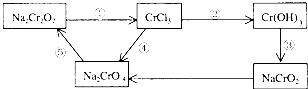
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当有0.2 mol CO2生成时,溶液中阴离子的物质的量增加l mol |
| B、该反应中,每有2mol CN-反应,转移电子为10 mol |
| C、上述反应中的还原剂是OH- |
| D、还原性:Cl->CN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com