
��8�֣��ɶ�����Ԫ����ɵ�A��B��C��D��E��F������������ֻ��C��D�Ƿ��ӣ��������־�Ϊ��һ����λ����ɵ������ӻ�һ����λ����ɵ������ӣ���ÿ�����ж�����10�����ӡ���֪A��E���ɷǽ���Ԫ����ɵ������ӣ��������������й�ϵ��
��A����B�� C��D�� B����E����2
C��D�� B����E����2 D��
D��
��ͨ���� ���£�C��һ����ɫ�̼�����ζ�����壬�ҿ�ʹʪ��ĺ�ɫʯ
���£�C��һ����ɫ�̼�����ζ�����壬�ҿ�ʹʪ��ĺ�ɫʯ ����ֽ������
����ֽ������
����F���ӵ���Һ�м���C��ˮ��Һ�������ɰ�ɫ����W��C��Һ��������Ҳ����ʧ���ټ��뺬����B���ӻ����E���ӵ���Һʱ������W������һ��������ܽ⣬��һ������²��ܽ⡣
��ش��������⣺
��1����A�����Ƽ���ѧʽ�ֱ�Ϊ �� ��
��2��C��ˮ��Һ�д��ڵķ������������� �֡�
��3��д����F�����C��ˮ��Һ��Ӧ�����ӷ���ʽ�� ��
��4������0.1mol F���ӵ�50mL��Һ�У����뺬1.5mol/L B���ӵ�200mLǿ����Һ������а�ɫ��������������û�����м��뺬1mol/L E���ӵ�ǿ����Һ����Ҫʹ����ǡ���ܽ⣬�����������Һ���������Ϊ mL��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011��2012��߶���ѧ�ڵ�Ԫ���Ի�ѧ�Ծ������˽� ѡ���ĵ����£� ���ͣ������
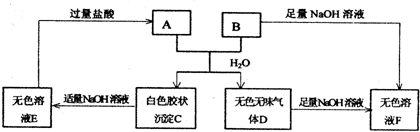
��12�֣��ɶ�����Ԫ����ɵ� A��B�����οɷ������б仯����B����ɫ��Ӧ�ʻ�ɫ��ͼ������������δ�г���
A��B�����οɷ������б仯����B����ɫ��Ӧ�ʻ�ɫ��ͼ������������δ�г���
��1��A��B�Ļ��������ˮ������Ӧ�����ӷ���ʽ______________________________��
��2��B��E����Һ��Ϸ�Ӧʱ���ɹ۲쵽��������__________________________��д���䷴Ӧ�����ӷ���ʽ__________________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com