
| A、多数合金的熔点一般比其各成分金属的熔点低 |
| B、多数合金的硬度一般比其各成分金属的硬度小 |
| C、合金的物理性质一般与其各成分金属的物理性质不同 |
| D、合金的化学性质一般与其各成分金属的化学性质不同 |


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl2溶液(FeCl3):加过量还原铁粉,过滤 |
| B、KNO3溶液(AgNO3):加过量KCl 溶液,过滤 |
| C、NaCl溶液(I2):加CCl4,分液 |
| D、KNO3溶液(NaCl):加热蒸发得浓溶液后,降温、过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 |
| B、用洁净铁丝蘸取两种样品在煤气火焰上灼烧,火焰颜色呈黄色的是小苏打 |
| C、分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 |
| D、先将两样品配成溶液,后分别加入石灰水,无白色沉淀生成的是小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:
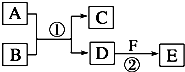 (A、B、C、D、E、F六种物质的转化关系如图(反应条件和部分产物未标出).
(A、B、C、D、E、F六种物质的转化关系如图(反应条件和部分产物未标出).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大力发展新能源是减少大气中SO2、NO2、可吸入颗粒物的措施之一 |
B、 在运输汽油的油罐车上所贴的化学危险标志如图 |
| C、为消除碘缺乏症,卫生部规定必须在食盐中加碘单质 |
| D、铜盐溶液都有毒,能使蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 事实 | 结论 |
| A | SiO2可用于制光导纤维 | SiO2有导电性 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | Cl2的水溶液可以导电 | Cl2是电解质 |
| D | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com