
 氮可形成多种氧化物,如NO、NO2、N2O4等.
氮可形成多种氧化物,如NO、NO2、N2O4等.| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
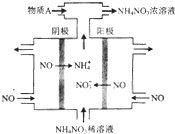
分析 (1)电解NO制备NH4NO3,由图可知,乙为阳极反应为:5NO-15e-+10H2O=5NO3-+20H+,甲为阴极反应为:3NO+15e-+18H+=3NH4++3H2O,电池总反应方程式为:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3;
(2)0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,由2NO2+2NaOH═NaNO3+NaNO2+H2O,得到溶液A中NaNO3物质的量浓度为0.1mol/L,NaNO2物质的量为0.1mol/L;
HNO2的电离常数Ka=7.1×10-4mol•L-1,CH3COOH的电离常数Ka=1.7×10-5mol•L-1,说明CH3COOH酸性小于HNO2的酸性,溶液中醋酸根离子水解程度小于亚硝酸根离子水解程度,溶液B碱性大于A溶液;
(3)①根据v=$\frac{△c}{△t}$计算v(N2O4),再利用速率之比等于化学计量数之比计算v(NO2);
60min、80min时N2O4的物质的量相等,说明60min时,反应到达平衡;
平衡时,N2O4的浓度为$\frac{0.08mol}{2L}$=0.04mol/L,NO2的浓度是$\frac{0.4mol}{2L}$-0.04mol/L×2=0.12mol/L,再根据K=$\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$计算平衡常数;
②若在相同条件下,最初向该容器充入的是N2O4气体,达到上述同样的平衡状态,为等效平衡,则N2O4完全转化可以得到0.4molNO2,平衡时N2O4的物质的量相等.
解答 解:(1)电解NO制备NH4NO3,由图可知,乙为阳极反应为:5NO-15e-+10H2O=5NO3-+20H+,甲为阴极反应为:3NO+15e-+18H+=3NH4++3H2O,电池总反应方程式为:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3,
故答案为:NH3;根据反应:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3;
(2)0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,由2NO2+2NaOH═NaNO3+NaNO2+H2O,得到溶液A中NaNO3物质的量浓度为0.mol/L,NaNO2物质的量为0.1mol/L,溶液B为0.1mol•L-1的CH3COONa溶液;
HNO2的电离常数Ka=7.1×10-4mol•L-1,CH3COOH的电离常数Ka=1.7×10-5mol•L-1,说明CH3COOH酸性小于HNO2的酸性,溶液中醋酸根离子水解程度小于亚硝酸根离子水解程度,溶液B碱性大于A溶液,两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为c(NO3-)>c(NO2-)>c(CH3COO-),
a.溶液B碱性大于A溶液,向溶液A中加适量水,稀释溶液,碱性减弱,不能调节溶液pH相等,故a错误;
b.向溶液A中加适量NaOH,增大碱性,可以调节溶液pH相等,故b正确;
c.向溶液B中加适量水,稀释溶液碱性减弱,可以调节溶液pH相等,故c正确;
d.溶液B碱性大于A溶液,向溶液B中加适量NaOH,溶液pH更大,故d错误;
故答案为:c(NO3-)>c(NO2-)>c(CH3COO-);bc.
(3)①20s内v(N2O4)=$\frac{\frac{0.05mol}{2L}}{\frac{1}{3}min}$=0.075mol/(L.s),速率之比等于化学计量数之比,v(NO2)=2v(N2O4)=0.15mol/(L.min);
60min、80min时N2O4的物质的量相等,说明60min时,反应到达平衡,所以n3=n4;
平衡时,N2O4的浓度为$\frac{0.08mol}{2L}$=0.04mol/L,NO2的浓度是$\frac{0.4mol}{2L}$-0.04mol/L×2=0.12mol/L,故平衡常数K=$\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$=$\frac{0.04}{0.1{2}^{2}}$=2.8,
故答案为:0.15;=;2.8;
②若在相同条件下,最初向该容器充入的是N2O4气体,达到上述同样的平衡状态,为等效平衡,则N2O4完全转化可以得到0.4molNO2,则N2O4的起始物质的量为$\frac{1}{2}$×0.4mol=0.2mol,N2O4的起始浓度为$\frac{0.2mol}{2L}$=0.1mol/L,平衡时N2O4的物质的量为0.08mol,故N2O4的转化率为$\frac{0.2mol-0.08mol}{0.2mol}$×100%=60%,
故答案为:0.1;60%.
点评 本题考查化学平衡计算与影响因素、化学平衡常数、盐类水解、离子浓度大小比较、电解原理等知识,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及灵活应用基础知识的能力,需要学生具备扎实的基础与灵活应用能力,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | CuO分别与稀硫酸、稀盐酸反应 | |
| B. | CaCO3、Na2CO3分别与盐酸反应 | |
| C. | H2SO4、K2SO4溶液分别与Ba(OH)2溶液反应 | |
| D. | Na分别与水、稀盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5:2 | B. | 3:1 | C. | 15:2 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
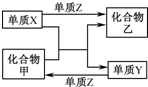 X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物.下表各组物质之间通过一步反应不能实现如图所示转化的是( )
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物.下表各组物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | X | Y | Z | 甲 | 乙 |
| A | Fe | H2 | O2 | H2O | Fe3O4 |
| B | Mg | C | O2 | CO2 | MgO |
| C | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
| D | Cl2 | N2 | H2 | NH3 | HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ca2+、Cl-、AlO2- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | NH4+.、Mg2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(HCO3)2溶液加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| B. | 向NH4HCO3溶液中滴入少量NaOH溶液:NH4++OH-═NH3•H2O | |
| C. | FeSO4溶液在空气中变黄色:4Fe2++O2+4H+═4Fe3++2H2O | |
| D. | 用NaOH溶液吸收NO2气体:3NO2+2NaOH═2NaNO3+NO↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com