
分析 主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍,W原子只能有2个电子层,最外层电子数为6,则W为O元素.X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍,即三元素原子序数之和为40,X若为第三周期元素,X、Y、Z的原子序数之和大于W原子序数的5倍,所以可以断定X也在第二周期,故X为F元素,则Y、Z原子序数之和=40-9=31,平均原子序数为15.5,可以推断Y处于第三周期、Z处于第四周期,Z的原子序数大于18,若Y为Na元素,则Z为Ca元素,若Y为Mg元素,则Z为K元素,X的原子序数再增大,不符合题意,由于元素W与Y形成的化合物M的熔点最高,故Y为Mg元素,Z为K元素,化合物M为MgO,据此解答.
解答 解:主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍,W原子只能有2个电子层,最外层电子数为6,则W为O元素.X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍,即三元素原子序数之和为40,X若为第三周期元素,X、Y、Z的原子序数之和大于W原子序数的5倍,所以可以断定X也在第二周期,故X为F元素,则Y、Z原子序数之和=40-9=31,平均原子序数为15.5,可以推断Y处于第三周期、Z处于第四周期,Z的原子序数大于18,若Y为Na元素,则Z为Ca元素,若Y为Mg元素,则Z为K元素,X的原子序数再增大,不符合题目中主族元素的要求,由于元素W与Y形成的化合物M的熔点最高,故Y为Mg元素,Z为K元素,化合物M为MgO.
(1)W为O元素,原子的L层电子排布式为 2s22p4,O3分子中中心氧原子价层电子对数=2+$\frac{6-2×2}{2}$=3、含有1对孤电子对,故O3空间构型为V形,
故答案为:2s22p4;V形;
(2)X单质为F2,与水发生反应:2F2+2H2O=4HF+O2,
故答案为:2F2+2H2O=4HF+O2;
(3)化合物M为MgO,属于离子化合物,由于MgO晶体中离子的电荷多、离子半径小,故MgO晶格能大,故MgO熔点较高;
在碳酸二甲酯分子中-OCH3,C原子4个单键,采取sp3杂化,在酯基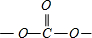 中,C原子成2个C-O单键、1个C=O双键,双键按单键计算,故中心C原子的杂化轨道数为3,采取sp2杂化,为平面正三角形,键角为120°,故O-C-O的键角约为120°,
中,C原子成2个C-O单键、1个C=O双键,双键按单键计算,故中心C原子的杂化轨道数为3,采取sp2杂化,为平面正三角形,键角为120°,故O-C-O的键角约为120°,
故答案为:MgO;MgO晶格能比NaCl的大;sp2和sp3;120°;
(4)F、Mg、K形成立方晶体结构的化合物,晶胞中F占据所有棱的中心,晶胞中F原子数目为12×$\frac{1}{4}$=3,Mg位于顶角,晶胞中Mg原子数目为8×$\frac{1}{8}$=1,K处于体心位置,晶胞中含有1个K原子,则该晶体的组成为F:Mg:K=3:1:1,
故答案为:3:1:1;
(5)含有元素K的盐的焰色反应为紫色,许多金属盐都可以发生焰色反应,其原因为:灼烧时电子从基态到激发态,激发态电子从能量较高的轨道跃迁到能量较低的轨道是,以一定波长光的形式释放能量,从而出现不同的颜色,
故答案为:紫;灼烧时电子从基态到激发态,激发态电子从能量较高的轨道跃迁到能量较低的轨道是,以一定波长光的形式释放能量.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、分子结构与性质、晶体类型与性质、晶胞计算等,难度中等,推断元素是解题的关键,要充分利用原子序数的关系结合周期表的结构进行判断元素.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8gNa2S和Na2O2的固体混合物中含有的阴离子数目为0.1NA | |
| B. | 用铜做电极电解CuSO4溶液的反应方程式:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 等质量的N2和CO所含原子数均为2NA | |
| D. | pH等于2的醋酸溶液中加入0.01mol/L的盐酸,溶液pH会变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
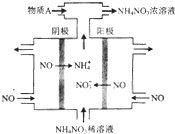 氮可形成多种氧化物,如NO、NO2、N2O4等.
氮可形成多种氧化物,如NO、NO2、N2O4等.| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、Cl-、Na+、NO3- | B. | K+、Na+、NO3-、HCO3- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Na+、Cl-、AlO2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2与水反应时,1 mol Na2O2转移1 mol电子 | |
| B. | 78gNa2O2含有阴、阳离子总数是4NA | |
| C. | 1mo1•L-1的AlC13溶液中,C1-离子的数目为3 NA | |
| D. | 5.6 g铁与足量盐酸反应转移的电子数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | |
| B. | 2Na2O2+2CO2═2NaCO3+O2 | |
| C. | Na2O2+H2SO4(稀)═Na2SO4+H2O2 | |
| D. | Fe2O3+3Na2O2(熔融)═2Na2FeO4十Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H>0表示放热反应,△H<0表示吸热反应 | |
| B. | 热化学方程式中的化学计量数只表示物质的量,可以是分数也可以是小数 | |
| C. | 1molH2SO4和1mo Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 | |
| D. | 1molH2和0.5mol O2反应放出的热就是H2的燃烧热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com